De scheikundige werking van een instant coldpack
 In de sportwereld wordt er regelmatig gebruik gemaakt van een instant coldpack om zwellingen bij blessures te voorkomen of te laten afnemen. Een instant coldpack bevat twee stoffen die bij samenvoeging een koudmakend mengsel vormen. De stoffen hebben dus energie (warmte) uit de omgeving nodig om te kunnen mengen. Deze warmte kunnen ze bijvoorbeeld halen van een omgeslagen voet die daardoor wordt afgekoeld en dus minder zal opzwellen.
In de sportwereld wordt er regelmatig gebruik gemaakt van een instant coldpack om zwellingen bij blessures te voorkomen of te laten afnemen. Een instant coldpack bevat twee stoffen die bij samenvoeging een koudmakend mengsel vormen. De stoffen hebben dus energie (warmte) uit de omgeving nodig om te kunnen mengen. Deze warmte kunnen ze bijvoorbeeld halen van een omgeslagen voet die daardoor wordt afgekoeld en dus minder zal opzwellen.
Inhoud
- Een koudmakend mengsel
- Invloed van intermoleculaire krachten
- Het streven naar meer wanorde
- Verschil met een ijszak
Een koudmakend mengsel
Een veel gebruikt instant coldpack bevat ammoniumnitraat (NH4NO3) en water (H2O). Beide stoffen bevinden zich in een plastic zakje gescheiden van elkaar in twee compartimenten. Wanneer je het zakje indrukt, beschadig je de scheiding tussen beide compartimenten en worden de stoffen samengevoegd. Hierbij ontstaat een koudmakend mengsel met een temperatuur van ongeveer -10°C. Er wordt tijdens het oplossen van beide stoffen warmte uit de omgeving opgenomen en alzo maakt het zakje zijn omgeving koud.Invloed van intermoleculaire krachten
Dat NH4NO3 en H2O een koudmakend mengsel vormen, is te verklaren op basis van de intermoleculaire krachten die heersen tussen beide stoffen. Intermoleculaire krachten zorgen ervoor dat stoffen bij elkaar blijven. Of twee stoffen mengbaar zijn, hangt af van de grootte van de intermoleculaire aantrekkingskrachten tussen de moleculen van dezelfde soort en van de grootte van de intermoleculaire aantrekkingskrachten tussen de twee stoffen.Watermoleculen vormen onderling zeer sterke waterstofbruggen.
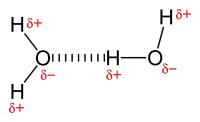 waterstofbruggen tussen watermoleculen / Bron: Publiek domein, Wikimedia Commons (PD)
waterstofbruggen tussen watermoleculen / Bron: Publiek domein, Wikimedia Commons (PD)Het streven naar meer wanorde
Je zal verwachten dat de intermoleculaire krachten tussen de twee stoffen minstens even sterk moeten zijn als deze tussen de individuele stoffen om vermenging te krijgen. Dit hoeft niet steeds waar te zijn. Er is ook nog zoiets als het streven naar een maximum aan wanorde. Het mengen van deeltjes zorgt voor meer wanorde dan wanneer de stoffen netjes in twee lagen blijven.Ondanks de zwakkere intermoleculaire krachten die na mengen ontstaan, zal ammoniumnitraat toch goed oplosbaar zijn in water, dit dus door de toegenomen chaos. Het moet hiervoor wel energie opnemen uit de omgeving. Het kost hier immers meer energie om gelijke moleculen uit elkaar te halen dan dat er energie vrijkomt bij het ontstaan van menginteracties. Het mengen heeft dus een sterke temperatuurafname als gevolg wat dit mengsel uitermate geschikt maakt om gebruikt te worden in een coldpack.
Verschil met een ijszak
Voor de koeling van een blessure kan uiteraard evengoed een ijszak worden gebruikt. Hiervoor moet je gewoon ijsblokjes uit de diepvriezer nemen. Er komt geen chemie aan te pas. Alhoewel een ijszak goedkoper is, blijft een instant coldpack toch handiger. Je kan het gemakkelijk vervoeren en het blijft gebruiksklaar bij elke omgevingstemperatuur.© 2020 - 2024 Guust2016, het auteursrecht van dit artikel ligt bij de infoteur. Zonder toestemming is vermenigvuldiging verboden. Per 2021 gaat InfoNu verder als archief, artikelen worden nog maar beperkt geactualiseerd.
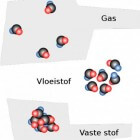 Aggregatietoestanden en intermoleculaire krachtenDe aggregatietoestand van een stof (vast, vloeibaar of gasvormig) staat in direct verband met de intermoleculaire kracht…
Aggregatietoestanden en intermoleculaire krachtenDe aggregatietoestand van een stof (vast, vloeibaar of gasvormig) staat in direct verband met de intermoleculaire kracht…
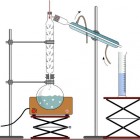 Het azeotroop gedrag van een ethanol-watermengselEen ethanol-watermengsel kan door middel van een destillatie nooit volledig worden gescheiden in zuivere ethanol en zuiv…
Het azeotroop gedrag van een ethanol-watermengselEen ethanol-watermengsel kan door middel van een destillatie nooit volledig worden gescheiden in zuivere ethanol en zuiv…
 De kationenuitwisselingscapaciteit van een bodemPlanten moeten voor hun groei kationen absorberen uit de bodem. Het is niet voldoende dat die kationen worden toegevoegd…
De kationenuitwisselingscapaciteit van een bodemPlanten moeten voor hun groei kationen absorberen uit de bodem. Het is niet voldoende dat die kationen worden toegevoegd…
 Gedemineraliseerd water makenLeidingwater wordt zelden gebruikt in laboratoria.De mineralen aanwezig in leidingwater kunnen chemische reacties immers…
Gedemineraliseerd water makenLeidingwater wordt zelden gebruikt in laboratoria.De mineralen aanwezig in leidingwater kunnen chemische reacties immers…
Gerelateerde artikelen
Verwerkbaarheid betonspecieVerwerkbaarheid is een algemeenbegrip. In principe worden die eigenschappen van betonspecie bedoeld, die te maken hebben…
Krachten SamenstellenOp een voorwerp worden meestal twee of meer krachten uitgeoefend. Je kunt deze krachten vervangen door één kracht, die h…
Bronnen en referenties
- Inleidingsfoto: KlausHausmann, Pixabay
- Afbeelding bron 1: Publiek domein, Wikimedia Commons (PD)
Guust2016 (74 artikelen)
Laatste update: 21-10-2020
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Laatste update: 21-10-2020
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Per 2021 gaat InfoNu verder als archief. Het grote aanbod van artikelen blijft beschikbaar maar er worden geen nieuwe artikelen meer gepubliceerd en nog maar beperkt geactualiseerd, daardoor kunnen artikelen op bepaalde punten verouderd zijn. Reacties plaatsen bij artikelen is niet meer mogelijk.