Wat zijn de risico’s van fijnstof in het milieu?
 Fijnstof is onder te verdelen in een primair en een secundair aërosol. Kijken we puur naar de milieueffecten van fijnstof, moeten we vooral naar de secundaire variant kijken. Secundaire deeltjes ontstaan meestal pas na enkele minuten of dagen, door (foto-)chemische reacties tussen (vooral) gasvormige luchtverontreinigingen.
Fijnstof is onder te verdelen in een primair en een secundair aërosol. Kijken we puur naar de milieueffecten van fijnstof, moeten we vooral naar de secundaire variant kijken. Secundaire deeltjes ontstaan meestal pas na enkele minuten of dagen, door (foto-)chemische reacties tussen (vooral) gasvormige luchtverontreinigingen.Omdat deze deeltjes zeer klein zijn, is de verblijftijd in de lucht relatief lang. Daarom is ook de doordringing in de longen groot en vormen ze een bedreiging voor de gezondheid. Deze fijnstof deeltjes zijn ook verantwoordelijk voor de heiigheid die zomers optreedt wanneer warm weer (fotochemie) met een verontreinigde lucht van het Europese continent wordt aangevoerd. Daarbij worden ook secundaire gasvormige verontreinigingen, zoals ozon (O3), gevormd.
Andere milieueffecten zijn voornamelijk verzuring en smog. Ook dit gebeurt nadat fijnstof reageert met andere deeltjes in het milieu. Hierbij spelen vooral de gassen ammoniak (NH3), stikstofoxiden (NOx), zwaveldioxide (SO2) en vluchtige organische koolwaterstoffen (VOS) een belangrijke rol.
Door de grote verscheidenheid van fijnstof zijn er moeilijk chemische en fysieke eigenschappen aan toe te kennen. En door deze grote verscheidenheid aan eigenschappen kan fijnstof ook voor veel verschillende milieuproblemen zorgen met als overkoepelend thema: de klimaatverandering. Indirect zorgt fijnstof ook voor de temperatuurstijging, ontbossing, stijging van de zeespiegel enz.
Om toch een beeld te krijgen van de risico’s van fijnstof in het milieu is hieronder een voorbeeld gekozen dat de duidelijkste resultaten op leveren ten aanzien van de hoeveelheid fijnstof. Het behoort nog altijd tot de secundaire fractie van fijnstof, maar het heeft een meer directere werking dan de meeste andere milieuprocessen.
Verzuring
Verzuring is het gevolg van verontreiniging van de lucht met stoffen (zwaveldioxide, stikstofoxiden en ammoniak) waaruit zuren gevormd kunnen worden, die via natte en droge depositie de bodem, water, planten en materialen kunnen aantasten.Droge depositie wil zeggen dat gassen of aerosolen direct vanuit de atmosfeer op de bodem deponeren. Er wordt van natte depositie gesproken als fijnstof via neerslag het aardoppervlak bereikt. Gebeurt dit via mist en dauw dan spreekt men van occulte depositie. De atmosfeer kun je grofweg in twee lagen verdelen. De bovenste laag is de wolkenlaag, waar de regendruppels gevormd worden. De onderste laag is de vergiftigde laag met giftige stoffen (SO2, HNO3, NH3, CO2, O3, H2O2, enz.) en fijnstof. De concentraties van de gassen en fijnstof veranderen niet in de tijd, alleen met hoogte. Als een regendruppel uit een wolk naar beneden valt zal het een fractie van de atmosferische aërosol opnemen die hij op zijn pad tegenkomt. Ook kan het atmosferische gassen absorberen. De zuurgraad van regenwater verandert voortdurend in de tijd en dus met hoogte. Dit komt door de opname van zure fijne stof deeltjes en neutrale componenten.
In de jaren zeventig kwam de verzuringsproblematiek hoog op de nationale en internationale agenda. In Duitsland ontstond namelijk grote bezorgdheid over de relatie tussen de afname van vitaliteit van bossen en zure regen. Omdat de effecten op bodem en ecosystemen als het centrale probleem beschouwd werd heeft de verzuring als milieuthema vooral betrekking op stoffen die door omzettingsprocessen in de bodem tot zuurvorming leiden. De belangrijkste verzurende stoffen zijn zwaveldioxide, stikstofoxiden en ammoniak en hun reactieproducten. Onder de reactieproducten vallen fijne stof deeltjes (NH4+, NO3- en SO42-).
Werkingsmechanisme
Fijne stof deeltjes reageren met de regendruppels in de onderste laag van de atmosfeer. Verdere analyses wijzen uit dat een fijnstofdeeltje met een lagere pH dan de regen een verzurend effect heeft op dat water. Andersom geldt ook dat een fijnstofdeeltje met een pH hoger dan het regenwater een neutraliserend effect heeft. Wel is het zo dat het verzurend effect nog altijd hoger ligt dan het neutraliserende effect. De concentratie van het fijnstof heeft een evenredige relatie met de mate waarin dat deeltje de H+ concentratie kan beïnvloeden. Hoe hoger de H+ concentratie, hoe zuurder de bodem. Voor de belangrijkste fijne stofdeeltjes (SO2, HNO3 en NH3) zijn de grafieken weergegeven met pH-waarde uitgezet tegen de desbetreffende concentratie. Regen met een pH tussen de 5 en de 6,5 wordt beschouwd als normaal. Alles daaronder wordt beschouwd als zure regen.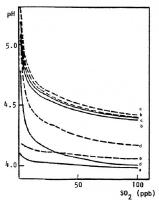
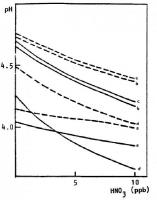
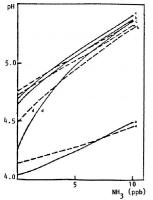
De grafieken laten duidelijk zien dat SO2 en HNO3 een verzurende werking hebben op de regendruppels. Daarentegen heeft NH3 een neutraliserende werking. NH3 kan namelijk een H+ deeltje opnemen en reageren tot NH4. Voor de andere twee reacties geldt dat er juist een H+ deeltje kan worden afgegeven. De belangrijkste hierbij horende reactievergelijkingen die in de atmosfeer plaatsvinden zijn hieronder opgesteld:
- SO2 + H2O ↔ H+ + HSO3-
- HNO3 ↔ H+ + NO3-
- NH3 + H2O ↔ OH- + NH4+
- NH3 + H+ ↔ NH4+
Dit wil niet zeggen dat de zuurgraad door zure depositie onmiddellijk toeneemt. De bodem heeft namelijk nog een buffercapaciteit door de aanwezigheid van onder andere aluminium en calcium. Deze buffercapaciteit verschilt vanzelfsprekend per bodemsoort.
Bij langdurige depositie van verzurende stoffen zal de buffercapaciteit echter uitgeput raken en zal de bodem zuurder worden. In bosbodems wordt een groot deel van de zure depositie door aluminium gebufferd. Bij de neutralisatie van het zuur komen aluminiumionen in het bodemvocht en uiteindelijk in het grondwater terecht. Deze verhoogde concentratie tast de wortelgroei aan en de opname van essentiële voedingsstoffen wordt bemoeilijkt. Verspreiding, omzetting en depositie van deze stoffen kan op een schaal van enkele kilometers tot vele duizenden kilometers uiteen lopen. Verzuring is daarom lang geen lokaal probleem, maar een nationaal of zelfs internationaal probleem.
De depositiesnelheid is dus afhankelijk van de chemische aard van het gas of deeltje, de fysische oplosbaarheid en de aerodynamische eigenschappen. Grote deeltjes hebben zoveel massa dat ze de snelle luchtbewegingen om bijvoorbeeld vegetatie niet kunnen volgen en daarom neerslaan op planten en dergelijke. Omgekeerd hebben kleine deeltjes ook een hoge diffusiesnelheid en zullen daarom snel het depositieoppervlak bereiken. In het middengebied (deeltjes tussen 0,1 en 1 micrometer) zijn de processen van neerslaan en diffusie weinig efficiënt en zal dus de depositiesnelheid laag zijn. Verblijftijden in de atmosfeer zijn voor deze stoffen dus lang. In deze groep stoffen zitten de secundaire, zure, aërosolen zoals die gevormd worden uit SOx, NOx en NH3. Door deze processen kan de afstand tussen bron en receptor variëren van enkele honderden meters (gasvormig NH3), via 50 tot 100 kilometer, voor SO2 tot duizenden kilometers voor geoxideerde stikstofverbindingen en aërosolen.
 Bron: Planbureau voor de Leefomgeving (PBL)
Bron: Planbureau voor de Leefomgeving (PBL)