Uranium: Het element
 Uranium met grootste atoomgewicht van voorkomende elementen, komt van nature voor in lage concentraties van enkele delen per miljoen in de bodem, rotsen en water, en wordt commercieel gewonnen uit uranium-dragende mineralen zoals uraninite. Ontdekking van uranium in de mineraal pitchblende door MH Klaproth in 1789, EM Péligot was de eerste het metaal te isoleren. Zijn radioactieve eigenschappen werden ontdekt in 1896 door H Becquerel. Onderzoek door E Fermi en anderen, zoals J. R Oppenheimer beginnend in 1934 leidde tot gebruik als brandstof in de nucleaire industrie en in de eerste nucleaire wapen gebruikt in oorlogstijd.
Uranium met grootste atoomgewicht van voorkomende elementen, komt van nature voor in lage concentraties van enkele delen per miljoen in de bodem, rotsen en water, en wordt commercieel gewonnen uit uranium-dragende mineralen zoals uraninite. Ontdekking van uranium in de mineraal pitchblende door MH Klaproth in 1789, EM Péligot was de eerste het metaal te isoleren. Zijn radioactieve eigenschappen werden ontdekt in 1896 door H Becquerel. Onderzoek door E Fermi en anderen, zoals J. R Oppenheimer beginnend in 1934 leidde tot gebruik als brandstof in de nucleaire industrie en in de eerste nucleaire wapen gebruikt in oorlogstijd.
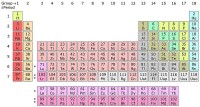 Periodiek systeem van elementen.Uranium atoomnummer 92 / Bron: Sandbh, Wikimedia Commons (CC BY-SA-4.0)
Periodiek systeem van elementen.Uranium atoomnummer 92 / Bron: Sandbh, Wikimedia Commons (CC BY-SA-4.0)Plaats van het element uranium in het periodiek systeem
Uranium is een scheikundig element met symbool U en atoomnummer 92. Een uranium atoom heeft 92 protonen en 92 elektronen, waarvan 6 valentie-elektronen.Het is een zwaar, zilverwit, zwak radioactief metaal uit de actiniden serie van het periodiek systeem. Het heeft een Mohs-hardheid van 6 voldoende om in glas te krassen en ongeveer gelijk aan de hardheid van titanium, rhodium, manganese and niobium. Het is buigzaam, kneedbaar, iets paramagnetische, sterk elektropositief en is een slechte elektrische geleider.Algemene eigenschappen van het element uranium
| Naam | Symbool | Atoomnummer | Groep | Periode | Blok | Reeks | Kleur | Magnetisme |
|---|---|---|---|---|---|---|---|---|
| Uranium | U | 92 | Scandiumgroep | periode 7 | F-blok | Actinide | Zilvergrijs | Licht paramagnetisch |
Chemische eigenschappen van het element Uranium
| Atoommassa (u) | Elektronen configuratie | Oxidatie toestanden | Elektro negativiteit (Pauling) | Atoomradius (pm) | Ionisatie energie (KJ/mol) |
|---|---|---|---|---|---|
| 238,02891 | [Rn] 5f3 6d1 7s2 Shell: 2,8,18,32,21,9,2 | 6, 5, 4, 3 Zwak basische oxide | 1,38 | Atoomrad: 156 Covalente rad: 196 +/-7 v/d Waals rad: 186 | 1e: 597 2e: 1420 |
Fysische eigenschappen van het element Uranium
| Dicht heid (0C) (g/cm3) | Smelt punt | Kook punt | Aggre gatie toestand | Smelt warmte (KJ/mol) | Verdamp ings warmte (KJ/mol) | Kristal structuur | Speci fieke warmte (J/kg.K) | Elek- trische weer stand (μΩ.cm) | Warmte geleid ing (W/m.K) |
|---|---|---|---|---|---|---|---|---|---|
| 19,1 | 1405.3 K 1132.2 °C 2070 °F | 4404 K 4131 °C 7468 °F | vast | 9.14 | 417.1 | Ortho- rombisch | 120 0 °C: | 0.280 | 27.5 |
Mechanische eigenschappen van het element Uranium
| Elasticiteits (Young)modules E (GPa) | Glijdings (shear)modules G (GPa) | Compressie (bulk)modules K (GPa) | Poisson (ratio)factor | Hardheid Mohs | Thermal expansion µm/m.K (at 25 °C) |
|---|---|---|---|---|---|
| 208 | 111 | 100 | 0,23 | 6,0 | 13.9 |
De isotopen van het element Uranium
- Uranium-238 is splijtbaar door snelle neutronen, en kan worden getransformeerd tot plutonium-239. Een andere splijtbare isotoop uranium-233, kan worden geproduceerd uit natuurlijke thorium en is eveneens van belang in de nucleaire technologie.
- Natuurlijk uranium bestaat uit drie belangrijke isotopen: uranium-238 (99,28% natuurlijke overvloed), uranium-235 (0,71%), en uranium-234 (0,0054%). Alle drie zijn radioactief, en zenden alfadeeltjes uit. (afbeelding alfa deeltje)
- Uranium-238 is de meest stabiele isotoop, met een halveringstijd van 4.5 × 10↑9 jaar, dat is gelijk aan de leeftijd van de aarde. Uranium-235 heeft een halfwaardetijd van ongeveer 7 × 10↑8 jaar, en uranium-234 een halfwaardetijd van 2,5 × 10↑5 jaar. Voor natuurlijk uranium, ongeveer 49% van de alfa-stralen worden uitgezonden door 238U atoom, en 49% door 234U en 2,0% door 235U.
- Uranium-238 is meestal een α straler, vervalt via de "Uranium Serie", die 18 "leden" telt die uiteindelijk vervallen tot lood-206.
- De verval reeks 235U, de actinium serie heet 15 leden, die uiteindelijk vervallen tot lood-207. Uranium-234 is een lid van de "Uranium Series", en vervalt tot lood-206 door een reeks van relatief kortlevende elementen. Uranium-233 ontstaat uit thorium-232 door neutronen bombardement in een kernreactor. 233U is splijtbaar, zijn verval serie eindigt met thallium-205.
- Uranium-235 is belangrijk voor de nucleaire reactoren en nucleaire wapens, want het is de enige uranium isotoop, bestaand in de natuur op aarde. Een significante hoeveelheid is splijtbaar. Dit betekent dat het kan in twee of drie fragmenten (splijtingsproducten) worden gesplitst door middel van thermische neutronen.
- Uranium-238 is niet splijtbaar, maar is een vruchtbaar isotoop, want na neutronen activerings analyse kan plutonium-239, een andere splijtbare isotoop produceren. kan de 238U kern een neutron absorberen om de radioactieve isotoop uranium-239 te produceren. 239U vervalt door de bèta-emissie tot neptunium-239, ook een bèta-straler die vervalt binnen een paar dagen tot plutonium-239. 239Pu werd gebruikt als splijtbaar materiaal in de eerste atoombom ontploft in de "Trinity test" in 1945 in New Mexico.
Stabielste isotopen van uranium
| Isotoop | RA(%) | Halveringstijd | Verval via | Vervalenergie | Vervalproducten |
|---|---|---|---|---|---|
| 233U | Synthetisch | 1,59x10↑3 jaar | alfa | 4,91 | 229Th |
| 234U | 0,0055 | 2,46x10↑5 jaar | alfa | 4,86 | 230Th |
| 235U | 0,721 | 7,038x10↑8 jaar | alfa | 4,68 | 231Th |
| 236U | Synthetisch | 2,34x10↑7 jaar | alfa | 4,57 | 232Th |
| 238U | 99,28 | 4, 468x10↑9 jaar | alfa | 4,27 | 234Th |
 Uranium-erts Uraniet / Bron: Kgrr, Wikimedia Commons (CC BY-SA-2.5)
Uranium-erts Uraniet / Bron: Kgrr, Wikimedia Commons (CC BY-SA-2.5)Het voorkomen van uranium
- Alle elementen zwaarder dan ijzer, zijn gevormd in supernova's.
- Uranium is zwak radioactief, omdat al zijn isotopen instabiel zijn. De meest voorkomende uranium isotopen in de natuur zijn uranium-238 (99,3%) van totaal aanwezige uranium; uranium-235 (0,7%) en uranium 234 (0,005%)
- Uranium vervalt langzaam door emissie van alfa deeltjes. De halfwaardetijd van uranium-238 is ongeveer 4,5 miljard jaar en dat van uranium-235 is 704 miljoen jaar.
- De economisch exploreerbare uranium reserves in erts wordt geschat op 5,5 miljoen ton, terwijl 35 miljoen ton wordt gezien als bronnen met redelijke vooruitzichten voor economische winning in de toekomst.
- Zeventien landen produceren geconcentreerde uraniumoxiden, met Canada (27,9%) en Australië (22,8%) Kazachstan (10,5%), Rusland (8,0%), Namibië (7,5%), Niger (7,4%), Oezbekistan (5,5%), de Verenigde Staten (2,5%), Argentinië (2,1%), Oekraïne (1,9%) en China (1,7%).
Kenmerkende eigenschappen
Uraniummetaal reageert met bijna alle niet-metalen elementen (met uitzondering van de edelgassen) en hun verbindingen. Reactiviteit neemt toe met de temperatuur. Zoutzuur en salpeterzuur lossen uranium op, maar niet-oxiderende zuren (uitzondering zoutzuur) reageren zeer langzaam met uranium.Wanneer uranium fijn verdeeld is kan het reageren met koud water; in de lucht, wordt uranium metaal bedekt met een donkere laag uraniumoxide.
Allotropische vormen van uranium
α (orthorhombic) tot 660 °Cβ (tetragonal) van 660 °C tot 760 °C
γ (body-centered cubic) van 760 °C tot smeltpuntin deze fase is het metaal het best te vervormen.
 Uranium glas / Bron: Jdrzej Peka, Wikimedia Commons (CC BY-SA-3.0)
Uranium glas / Bron: Jdrzej Peka, Wikimedia Commons (CC BY-SA-3.0)Toepassingen van uranium
- Uranium-238 is splijtbaar door snelle neutronen, het kan worden getransformeerd tot plutonium-239. Een andere splijtbare isotoop uranium-233, kan worden geproduceerd uit natuurlijk thorium en is eveneens van belang in de nucleaire technologie.
- Uranium wordt gebruikt als kleurstof in uraniumglas produceren oranje-rood tot geel tinten citroen. Het werd ook gebruikt voor het kleuren en schaduwen in vroegere fotografie.
- Door zijn hoge dichtheid, wordt dit materiaal toegepast in traagheidsnavigatiesystemen en de gyroscopische kompas. Verarmd uranium heeft voorkeur boven vergelijkbare zware metalen omdat het gemakkelijk bewerkt en gegoten kan worden en de kosten relatief laag zijn. De belangrijkste risico van blootstelling aan verarmd uranium is chemische vergiftiging door uraniumoxide in niet de zwakke reactiviteit van uranium (uranium is een zwakke alfa-straler).
- Tijdens de Tweede Wereldoorlog, de hele Koude Oorlog, is uranium-235 gebruikt als de splijtbaar materiaal om kernwapens te produceren. Aanvankelijk, twee belangrijke types van kern(splijting)bommen werden gebouwd: een relatief eenvoudig apparaat dat gebruik maakt van uranium-235 en een meer gecompliceerde mechanisme dat gebruik maakt van plutonium-239 afkomstig van uranium-238 verval.
- De belangrijkste toepassing van uranium in de militaire sector is in penetratoren. Deze munitie bestaat uit verarmd uranium gelegeerd met 1-2% andere elementen. Bij hoge botssnelheid, de dichtheid, hardheid en zelfontbrandbaarheid van het projectiel is het mogelijk gepantserde doelen te vernietigen. Tank pantsers en andere verwijderbare bepantsering van voertuigen worden ook gehard met verarmd uranium platen.
- Het gebruik van verarmd uranium werd politiek en ecologisch omstreden na het gebruik van munitie met verarmd uranium door de VS, het Verenigd Koninkrijk en andere landen tijdens de oorlogen in de Perzische Golf en de Balkan werden vragen gesteld over uranium verbindingen in de grond.
- Verarmd uranium wordt ook gebruikt als een afscherming materiaal in een aantal containers die worden gebruikt voor het opslaan en vervoeren van radioactieve materialen. Terwijl het metaal zelf radioactief is, maakt zijn hoge dichtheid het effectiever dan lood in het stoppen van de straling uit bronnen zoals het radium.
- Een waterstofbom (H bom) is een atoombom die veruit het grootste deel van zijn explosieve energie uit kernfusie van waterstofatomen tot helium verkrijgt. Meestal worden de waterstofisotopen deuterium en/of tritium en verder lithium gebruikt. Dit zijn lichte kernen die relatief gemakkelijk fuseren. In de praktijk is een op kernsplijting uranium bom nodig om de temperatuur en druk te verkrijgen om het kernfusieproces in de thermonucleaire (waterstof) bom op gang te brengen.
Industrie
- Het belangrijkste gebruik van uranium is als brandstof in kerncentrales. Een kilo uranium-235 kan bij volledige splitsing ongeveer 2 × 10↑13 joule aan energie leveren, dat komt overeen met de energie inhoud van 1500 ton kolen.
- Kerncentrales gebruiken brandstof die meestal wordt verrijkt tot ongeveer 3% uranium-235. In sommige reactoren kan uranium-238 worden omgezet in plutonium.
- Vóór de ontdekking van radioactiviteit, werd uranium gebruikt in kleine hoeveelheden voor geel glas en glazuur voor aardewerk. De ontdekking van radium in uraniumerts verplaatste de aandacht van uranium naar het radium, die werd gebruikt om lichtgevende verf te vervaardigen. Er was drie ton uranium nodig voor een gram radium. Dit uranium "afval" ging naar de beglazing industrie, waardoor uranium glazuur goedkoop was en populair. Aardewerk- en tegel glazuur op bases van uranium houdende stof was het grootste deel van het gebruik.
- Uranium werd gebruikt in de fotografie, (uraniumnitraat als toner), in de leer en hout industrie voor kleurstoffen. Uraniumzouten zijn beitsen van zijde en wol. Uranylacetaat en uranylformiaat worden gebruikt in transmissie elektronenmicroscopie, om het contrast van biologische monsters en kleuring van virussen, geïsoleerde celorganellen en macromoleculen te verhogen.
- De ontdekking van de radioactiviteit van uranium luidde aanvullende wetenschappelijke en praktische toepassingen van het element. De lange halfwaardetijd van het isotoop uranium-238 (4,5 × 10↑9 jaar) maakt het geschikt voor het gebruik in het schatten van de leeftijd van gesteenten. Uranium metaal wordt gebruikt voor het maken van hoog-energetische röntgenstraling.
Kernsplijting
Een team onder leiding van Enrico Fermi in 1934 constateerde dat het bombarderen van uranium met neutronen, de emissie van bètastraling (elektronen of positronen) bevordert. De splijtingsproducten waren in eerste instantie aangezien voor de nieuwe elementen. De experimenten die leiden tot de ontdekking van kernsplijting, d.w.z. splitsen in lichtere elementen met vrijkomen van bindingsenergie werden uitgevoerd door Otto Hahn en Fritz Strassmann in Berlijn. Men noemde het proces in februari 1939 "kernsplitsing".Kort na Fermi hypothese dat de splijting van uranium genoeg neutronen vrij maakt om een continue kern(splijting) te onderhouden, werd dit bevestigd in 1939. Men vond dat gemiddeld 2,5 neutronen vrij kwam bij splijting van de zeldzame isotoop uranium-235. Verdere werkzaamheden bleek dat de veel voorkomende uranium-238 isotoop kan worden omgevormd in plutonium, die net als uranium-235, ook splijtbaar was door thermische neutronen. Deze ontdekkingen leidden tal van landen tot de ontwikkeling van kernwapens en kernenergie.
Op 2 december 1942, als onderdeel van het Manhattan Project, een ander team onder leiding van Enrico Fermi was in staat om de eerste zichzelf onderhoudende nucleaire kettingreactie te starten.
 Little boy / Bron: National Archives and Records Administration, Wikimedia Commons (Publiek domein)
Little boy / Bron: National Archives and Records Administration, Wikimedia Commons (Publiek domein)Twee types van atoombommen werden ontwikkeld door de Verenigde Staten tijdens de Tweede Wereldoorlog: een-uranium-apparaat "Little Boy", waarvan de splijtstof hoog verrijkt uranium was, en "Fatman" een op plutonium gebaseerde bom, waarvan plutonium was afgeleid van uranium-238. Het op uranium gebaseerde "Little Boy" werd de eerste nucleaire wapen gebruikt in de oorlog. De drukgolf en hitte golf van de bom vernietigt 50.000 gebouwen en doodt 75.000 mensen.
Kernreactoren
- Uranium-235 was de eerste isotoop, die splijtbaar bleek te zijn. Bij het bombardement met langzame neutronen, zal de kern splitsen in twee kleinere kernen, waarbij nucleaire bindingsenergie en extra neutronen vrij komen. Deze vrije neutronen bestoken andere uranium-235 kernen, die ook splijten in kleinere kernen, en een nucleaire kettingreactie treedt op die leidt tot grote warmte ontwikkeling die water omzet in stoom, die een turbine aandrijft waarmee stroom opgewekt wordt. De snelheid van de kettingreactie wordt geregeld door een neutronen absorberende stof die deel uit maakt van de regelstaven in de reactor.
- De X-10 Graphite Reactor in het Oak Ridge National Laboratory was 's werelds tweede kernreactor (na Enrico Fermi's Chicago Pile) en was de eerste reactor ontworpen en gebouwd voor continu gebruik.
- Argonne National Laboratory's Experimental kweekreactor werd de eerste kernreactor om elektriciteit op te wekken in 1951. De stad Arco werd de eerste in de wereld die al zijn elektriciteit uit kernenergie haalde.
- Eerste commerciële kerncentrale in de Sovjet-Unie, begon met zijn reactor AM-1 in 1954
- Andere vroege kerncentrales werden Calder Hall in Engeland, die generatie begon in 1956
- Kernenergie gebruikt voor de eerste keer voor de voortstuwing van een onderzeeër, namelijk de USS Nautilus, in 1954.
Reactor Petten
De hogefluxreactor HFR in Petten (sinds 1960) is geen energiecentrale maar produceert radionucliden (radioactieve isotopen) die na chemische bewerkingen geleverd worden aan ziekenhuizen voor medisch gebruik, voor diagnostiek en voor de bestrijding van kanker (radiotherapie). De reactor in Petten produceert een derde van de wereldwijde behoefte aan medische isotopen. De medische activiteiten gebruiken ongeveer de helft van de capaciteit van de HFR, de andere helft wordt gebruikt voor onderzoek. Dit onderzoek betreft het gedrag van materialen onder invloed van ioniserende straling, metaalkundige kennis die belangrijk is voor de veiligheid van nucleaire installaties.Invloed uranium op Milieu en volksgezondheid
- Het verval van uranium, thorium en kalium-40 in de aardmantel is waarschijnlijk de energie bron die de mantel van de kern vloeibaar houdt en de convectie aandrijft die verantwoordelijk is voor de beweging van de tektonische platen en dus voor de beweging van de continenten.
- Uranium is overvloediger in de aardkorst aanwezig als antimoon, tin, cadmium, kwik, of zilver, het is net zo overvloedig als arseen of molybdeen. Uranium is te vinden in honderden mineralen waaronder uraninite (de meest voorkomende uranium erts), carnotiet, autunite, uranophane, Torbernite en coffinite
- Planten absorberen een deel van uranium uit de bodem. De concentratie uranium in planten varieert van 5 tot 60 delen per miljard, in as van verbrand hout is de concentratie circa 4 ppm.
- Een persoon kan worden blootgesteld aan uranium,of aan radioactieve vervalproducten zoals radon, door het inademen van stof of door inname van besmet water en voedsel.
- De hoeveelheid uranium in de lucht is klein, maar mensen die werken in fabrieken die fosfaat meststoffen verwerken, wonen in een omgeving waar kernwapens zijn getest, of waar een reactor ongeluk plaats vond, kan blootgesteld worden aan verhoogde concentratie uranium.
- De meeste ingenomen uranium wordt uitgescheiden. Slechts 0,5% wordt geabsorbeerd van de onoplosbare verbindingen van uranium, zoals oxiden. De absorptie van oplosbare uranyl ion kan tot 5% oplopen, maar de oplosbare uraniumverbindingen worden snel door het lichaam afgevoerd. Onoplosbare uraniumverbindingen vormen een gevaar, wegens bio-accumulatie blijft de stof jarenlang in botweefsel.
- Uranium wordt niet geabsorbeerd dwars door de huid, alfa-deeltjes die vrijkomen bij uranium zijn te groot en te langzaam om de huid te doordringen, de radioactieve straling van het metaal uranium is niet de kwaaie pier.
- Bovengrondse kernproeven door de Sovjet-Unie en de Verenigde Staten in de jaren 1950 en vroege jaren 1960 en Frankrijk in de jaren 1970 en 1980 verspreidde een aanzienlijke hoeveelheid neerslag van vervalproducten. Extra vervuiling is opgetreden van meerdere nucleaire ongelukken.
- Van Uranyl UO2 ionen, zoals van uraniumtrioxide of uranylnitraat en andere uranium verbindingen is aangetoond dat ze aangeboren afwijkingen, en immuunsysteem schade bij proefdieren veroorzaken. Studie gepubliceerd dat geen mens kanker heeft als gevolg van blootstelling aan natuurlijke of verarmd uranium. Blootstelling aan vervalproducten van uranium zoals radon, zijn wel een gezondheidsrisico. Uranium mijnwerkers hebben een hogere kans op kanker. Het functioneren van de nieren, hersenen, lever, hart, en andere systemen kunnen worden beïnvloed door blootstelling aan uraniumverbindingen.
- Inademen van uraniumhexafluoride heeft geleid tot slachtoffers, echter die sterfgevallen wijt men aan het giftige fluorwaterstofzuur en uranylfluoride, niet aan het uranium.
- Fijn verdeeld uraniummetaal levert brandgevaar omdat kleine korrels spontaan kunnen ontbranden in lucht bij kamertemperatuur.
© 2014 - 2025 Custor, het auteursrecht van dit artikel ligt bij de infoteur. Zonder toestemming is vermenigvuldiging verboden. Per 2021 gaat InfoNu verder als archief, artikelen worden nog maar beperkt geactualiseerd.
 Kernenergie, wat is het precies? En kunnen we zonder?Sinds de kernramp in Fukushima worden mensen weer eens met hun neus op de feiten gedrukt: kernenergie kan levensgevaarli…
Kernenergie, wat is het precies? En kunnen we zonder?Sinds de kernramp in Fukushima worden mensen weer eens met hun neus op de feiten gedrukt: kernenergie kan levensgevaarli…
 Beleggen in uraniumHet beleggen in uranium was een populaire vorm van beleggen. Er kon goed geld mee worden verdiend. Dat kwam omdat er een…
Beleggen in uraniumHet beleggen in uranium was een populaire vorm van beleggen. Er kon goed geld mee worden verdiend. Dat kwam omdat er een…
 De gevaren van kernenergie en kerncentralesKerncentrales vormen een gevaar voor de maatschappij en de samenleving. Althans dat beweren de tegenstanders van kernene…
De gevaren van kernenergie en kerncentralesKerncentrales vormen een gevaar voor de maatschappij en de samenleving. Althans dat beweren de tegenstanders van kernene…
 Chloroform in onze leefomgevingChloroform is een chemische stof die vooral bekend staat om zijn handige werking als anestheticum en zijn toepassingen b…
Chloroform in onze leefomgevingChloroform is een chemische stof die vooral bekend staat om zijn handige werking als anestheticum en zijn toepassingen b…
 Het aantonen van goudGoud is te zacht voor het maken van bijvoorbeeld sieraden. Door te legeren met bepaalde elementen zoals zilver, platina,…
Het aantonen van goudGoud is te zacht voor het maken van bijvoorbeeld sieraden. Door te legeren met bepaalde elementen zoals zilver, platina,…
Gerelateerde artikelen
Organisaties tegen kernenergieNadat het jarenlang toch tamelijk rustig was rondom kerncentrales en kernenergie, Nederland tot uitbreiding van kerncent…
Bronnen en referenties
- http://www.newstalk650.com/story/northern-saskatchewan-first-nation-signs-uranium-mining-deal-worth-600-million
- http://en.wikipedia.org/wiki/Uranium
- http://www.williammaloney.com/Aviation/USNavyMuseum/Aircraft/pages/12LittleBoyAtomicBomb.htm
- http://news.nost.jp/2010/12/zeldzame-en-schaarse-metalen/
- http://sciencenotes.org/?attachment_id=320
- Afbeelding bron 1: Sandbh, Wikimedia Commons (CC BY-SA-4.0)
- Afbeelding bron 2: Kgrr, Wikimedia Commons (CC BY-SA-2.5)
- Afbeelding bron 3: Jdrzej Peka, Wikimedia Commons (CC BY-SA-3.0)
- Afbeelding bron 4: National Archives and Records Administration, Wikimedia Commons (Publiek domein)
Custor (173 artikelen)
Laatste update: 19-02-2017
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 9
Laatste update: 19-02-2017
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 9
Per 2021 gaat InfoNu verder als archief. Het grote aanbod van artikelen blijft beschikbaar maar er worden geen nieuwe artikelen meer gepubliceerd en nog maar beperkt geactualiseerd, daardoor kunnen artikelen op bepaalde punten verouderd zijn. Reacties plaatsen bij artikelen is niet meer mogelijk.