Jodo-jodimetrie, een veelzijdige techniek
 Jodo-jodimetrie is een redoxmethode gebaseerd op titrimetrie. De methode kan worden gebruikt voor tal van toepassingen wegens het chemisch karakter van het betrokken redoxkoppel (dijood-jodide). Door de milde redox-eigenschappen van beide stoffen kunnen met deze methode immers concentraties van zowel sterke reductoren als sterke oxidatoren worden bepaald.
Jodo-jodimetrie is een redoxmethode gebaseerd op titrimetrie. De methode kan worden gebruikt voor tal van toepassingen wegens het chemisch karakter van het betrokken redoxkoppel (dijood-jodide). Door de milde redox-eigenschappen van beide stoffen kunnen met deze methode immers concentraties van zowel sterke reductoren als sterke oxidatoren worden bepaald.
- Redoxtitratie
- Jodo-jodimetrie
- Rechtstreekse titratie met I2
- Voorbeeld: bepaling van een vitamine C-gehalte
- Terugtitratie met I-
- Voorbeeld: bepaling van het gehalte hypochloriet in javel
Redoxtitratie
Een titratie is een volumetrische methode om de concentratie van een bepaalde opgeloste stof in een oplossing te bepalen. Door te bepalen hoeveel titreervloeistof (titrant) met exact gekende concentratie moet worden toegevoegd om al de stof te laten wegreageren, kan de concentratie van de stof berekend worden. Het moment waarop de stof volledig is weggereageerd, wordt het equivalentiepunt van de titratie genoemd. Dit equivalentiepunt kan duidelijk worden gemaakt door een kleurverandering van één van de chemicaliën zelf of door de kleurverandering van een toegevoegde indicator. Als de titratie gebaseerd is op een redoxreactie, dan spreekt men van een redoxtitratie.Jodo-jodimetrie
Jodo-jodimetrie is een redoxtitratie die steunt op de omzetting 2I- = I2 + 2e-. Wegens de middelmatige waarde van de normpotentiaal (E°(I2/2I-) = 0.54V), weten we dat I2 geen uitermate sterke oxidator is. Ook weten we uit deze normpotentiaal dat I- geen uiterst zwakke reductor is. I2 kan dus optreden als oxidator voor een sterke reductor maar I- kan evenzeer optreden als reductor voor een sterke oxidator. Met jodo-jodimetrie kan men dus zowel concentraties van sterke reductoren (met I2) als concentraties van sterke oxidatoren (met I-) bepalen.Rechtstreekse titratie met I2
Door een rechtstreekse titratie met I2 kunnen concentraties van sterke reductoren worden bepaald. Van de te bepalen reductor-oplossing wordt er een exact bepaald volume in een erlenmeyer gebracht. Vervolgens wordt de I2-oplossing met exact gekende concentratie druppelsgewijs en onder roeren toegevoegd via een buret. Bij het equivalentiepunt zal de reductor volledig zijn weggereageerd en zal er bij verdere toevoeging van I2 dus geen reactie meer kunnen doorgaan. Daar I2 geel gekleurd is, zal bij verdere toevoeging ervan de oplossing in de erlenmeyer geel kleuren. Het eindpunt van deze titratie kan visueel worden versterkt door toevoeging van zetmeel. Zetmeel geeft in aanwezigheid van I2 namelijk een diepblauw gekleurde oplossing.Voorbeeld: bepaling van een vitamine C-gehalte
Vitamine C en dijood (I2) reageren met elkaar in een 1-1-verhouding. Dit betekent dat één molecule vitamine C reageert met één molecule I2. Voor de bepaling doe je een exact afgemeten volume van de vitamine C-oplossing in een erlenmeyer en voeg je er enkele mL van een zetmeeloplossing aan toe. Je vult de buret met een I2-oplossing met exact gekende concentratie. Je voegt I2 uit de buret toe aan de vitamine C-oplossing tot de oplossing blauw kleurt.Rekenvoorbeeld:
Aan 30 mL van een vitamine C-oplossing moet er 20 mL van een I2-oplossing met een concentratie van 0.004 mol/l worden toegevoegd om een kleuromslag te krijgen.
→ VvitamineC-oplossing = 0.03 L
→ cI2 = 0.004 mol/L
→ VI2 = 0.02 L
Hieruit kan je berekenen hoeveel I2 je hebt toegevoegd aan de oplossing.
→ nI2 = cI2 . VI2 = 0.004 mol/L . 0.02 L = 0.00008 mol.
Omdat er volgens de reactievergelijking voor elk vitamine C molecule 1 molecule I2 nodig is, zat er bij deze bepaling dus 0.00008 mol vitamine C in de erlenmeyer, d.i. in 30 mL van de vitamine C-oplossing.
→ cvitamine C-oplossing = 0.00008 mol/0.03 L = 0.0027 mol/L
Meestal wordt een vitamine C-gehalte in bijvoorbeeld een vruchtensap uitgedrukt in mg vitamine C/100 mL sap.
Met Mvitamine C(molaire massa) = 176 g/mol kan je het gehalte uit het rekenvoorbeeld omzetten in deze eenheid.
→ (0.0027mol/L.176 g/mol = 0.475 g/L = 0.0475 g/100 mL = 47.5 mg/100 mL
Deze waarde komt overeen met een normaal gehalte vitamine C in vers sinaasappelsap.
Terugtitratie met I-
Voor de bepaling van de concentratie van een sterke oxidator kan er niet rechtstreeks worden getitreerd met jodide (I-). Het toevoegen van I- aan een oxidator geeft onmiddellijk een bruine kleur welke steeds intenser zal worden omdat er steeds meer I2 wordt gevormd. Bij het equivalentiepunt zal al de oxidator omgezet zijn en zal er dus geen I2 meer kunnen worden bijgevormd. Het equivalentiepunt wordt bereik als de kleurintensiteit maximaal is. Dit maximum is echter niet met het blote oog aan te tonen. Vandaar dat de bepaling van een oxidator met een terugtitratie dient te gebeuren. Er wordt hierbij een overmaat KI toegevoegd. Een gedeelte van de I--ionen zal worden omgezet in I2, waarvan het gehalte vervolgens kan worden bepaald door titratie met een thiosulfaat (S2O32-)-oplossing.2I- + oxidator → I2 + reductor
I2 + 2S2O32- → 2I- + S4O62-
I2 + 2S2O32- → 2I- + S4O62-
Uit de titratie kan dus het gehalte aan I2 worden bepaald. Dit gehalte staat rechtstreeks in verband met het gehalte oxidator.
Voorbeeld: bepaling van het gehalte hypochloriet in javel
Voor de bepaling doe je een exact afgemeten volume javel in een erlenmeyer en je voegt hierbij een overmaat KI-oplossing. De hypochloriet (ClO-) uit de javel zal hierbij reageren met het toegevoegde I-. Beide stoffen reageren met elkaar in een 1-2-verhouding.Dit betekent dat één molecule ClO- reageert met twee moleculen I-.H2O + ClO- + 2I- → Cl- + I2 + 2OH-
Tijdens de toevoeging van I- aan javel ontstaat er I2, wat ervoor zorgt dat de oplossing bruin kleurt. Je vult de buret met een thiosulfaat (S2O32-)-oplossing met een exact gekende concentratie. Je voegt deze oplossing toe aan de erlenmeyer tot de oplossing in de erlenmeyer ontkleurt. Tijdens de titratiereactie reageert het bruine I2 met het toegevoegde S2O32- tot het kleurloze I-. Wanneer al het I2 is weggereageerd, zal de oplossing dus ontkleurd zijn. Ook hier kan het visueel effect versterkt worden door de toevoeging van zetmeel. S2O32- reageert met I2 in een 2-1-verhouding. Dit betekent dat één I2-molecule reageert met twee moleculen S2O32-.
I2 + 2S2O32- → 2I- + S4O62-
Rekenvoorbeeld:
Aan 10 mL van een 10 keer verdunde javeloplossing wordt er een overmaat I- toegevoegd. Aan de verkregen I2-oplossing moet er 30mL van een S2O32- -oplossing met een concentratie van 0.05 mol/L worden toegevoegd voor ontkleuring.
→ cS2O32- = 0.05 mol/L
→ VS2O32- = 0.03L
Hieruit kan je berekenen hoeveel S2O32- je hebt toegevoegd aan de oplossing.
→ nS2O32- = cS2O32- . VS2O32- = 0.05mol/L . 0.03L = 0.0015 mol.
Omdat er volgens de reactievergelijking voor elk I2 molecule 2 moleculen S2O32- nodig zijn, zal er bij deze bepaling 0.00075 mol I2 in de erlenmeyer zitten. Omdat je weet dat er voor elk molecule ClO- 1 molecule I2 werd gevormd, weet je dus ook dat er 0.00075 mol ClO- in de 10 mL verdunde javel zat.
→ cClO- (verdunde javel) = 0.00075 mol/0.01 L = 0.075 mol/L
→ cClO-(javel) = 0.075 mol/L . 10 = 0.75 mol/L
Meestal wordt een NaClO-gehalte uitgedrukt in mNaClO/mjavel
Met MNaClO(molaire massa) = 74.44 g/mol kan je het gehalte uit het rekenvoorbeeld omzetten in deze eenheid.
→ (0.75 mol/L.74.44 g/mol = 55.83 g/L = 5.583 g/100mL ≈ 5.583 mg/100g
Deze waarde komt ongeveer overeen met het gehalte in gewoon commercieel javelwater.
© 2020 - 2024 Guust2016, het auteursrecht van dit artikel ligt bij de infoteur. Zonder toestemming is vermenigvuldiging verboden. Per 2021 gaat InfoNu verder als archief, artikelen worden nog maar beperkt geactualiseerd.
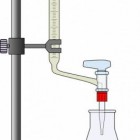 De werking van een redoxindicatorOm het equivalentiepunt bij een redoxtitratie met kleurloze of weinig gekleurde oplossingen te kunnen zien, dient een re…
De werking van een redoxindicatorOm het equivalentiepunt bij een redoxtitratie met kleurloze of weinig gekleurde oplossingen te kunnen zien, dient een re…
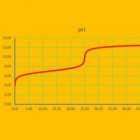 Titratiecurven in Excel: zwak zuur met sterke baseTitratiecurven geven een goed inzicht in de verandering van de pH tijdens de titratie. Rondom het equivalentiepunt treed…
Titratiecurven in Excel: zwak zuur met sterke baseTitratiecurven geven een goed inzicht in de verandering van de pH tijdens de titratie. Rondom het equivalentiepunt treed…
 Conductometrie als alternatief voor zuur-basetitratiesEen conductometrische titratie is een volumetrische concentratiebepaling waarbij de geleidbaarheid van het reactiemengse…
Conductometrie als alternatief voor zuur-basetitratiesEen conductometrische titratie is een volumetrische concentratiebepaling waarbij de geleidbaarheid van het reactiemengse…
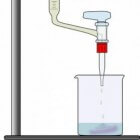 Titratiecurven in Excel: sterk zuur met sterke baseBij de titratie van een zuur met een base is het equivalentiepunt zichtbaar te maken met een indicator. Dat komt omdat i…
Titratiecurven in Excel: sterk zuur met sterke baseBij de titratie van een zuur met een base is het equivalentiepunt zichtbaar te maken met een indicator. Dat komt omdat i…
 Alcoholcontrole: hoe werkt een alcoholtest?Sinds 1939 is het strafbaar om dronken plaats te nemen achter het stuur. Aanvankelijk werd er hierop echter maar weinig…
Alcoholcontrole: hoe werkt een alcoholtest?Sinds 1939 is het strafbaar om dronken plaats te nemen achter het stuur. Aanvankelijk werd er hierop echter maar weinig…
 Redoxvergelijkingen opstellen vanaf nulAls je een redoxreactie uitvoert, kan je op basis van de waarnemingen meestal wel de eindproducten afleiden. Vervolgens…
Redoxvergelijkingen opstellen vanaf nulAls je een redoxreactie uitvoert, kan je op basis van de waarnemingen meestal wel de eindproducten afleiden. Vervolgens…
Gerelateerde artikelen
Bronnen en referenties
- Inleidingsfoto: OpenClipart-Vectors, Pixabay (bewerkt)
- Analytische scheikunde, W. Biermans, A. Pyra en F. Schuyten
Guust2016 (74 artikelen)
Laatste update: 09-07-2020
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Laatste update: 09-07-2020
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Per 2021 gaat InfoNu verder als archief. Het grote aanbod van artikelen blijft beschikbaar maar er worden geen nieuwe artikelen meer gepubliceerd en nog maar beperkt geactualiseerd, daardoor kunnen artikelen op bepaalde punten verouderd zijn. Reacties plaatsen bij artikelen is niet meer mogelijk.