Bismuth: Het element
 Bismut is een wit, kristallijn, broos metaal met een roze-achtige tint. De thermische geleidbaarheid is zeer laag, bij een hoge elektrische weerstand. Bismuth is bestendig t.a.v. zuurstof, water en lucht. Het heeft een lage toxiteit voor een zwaar metaal. Vanwege de toxiciteit van lood wordt steeds vaker overgegaan op bismuth. De variatie in de dikte van de oxidelaag veroorzaakt in het reflecterende licht verschillende golflengten en het kristal schittert in alle kleuren van de regenboog (prismawerking).
Bismut is een wit, kristallijn, broos metaal met een roze-achtige tint. De thermische geleidbaarheid is zeer laag, bij een hoge elektrische weerstand. Bismuth is bestendig t.a.v. zuurstof, water en lucht. Het heeft een lage toxiteit voor een zwaar metaal. Vanwege de toxiciteit van lood wordt steeds vaker overgegaan op bismuth. De variatie in de dikte van de oxidelaag veroorzaakt in het reflecterende licht verschillende golflengten en het kristal schittert in alle kleuren van de regenboog (prismawerking).
Plaats van bismuth in het periodiek systeem
 Periodiek systeem van elementen.Bismuth atoomnummer 83 / Bron: Kushboy, Wikimedia Commons (CC BY-SA-3.0)
Periodiek systeem van elementen.Bismuth atoomnummer 83 / Bron: Kushboy, Wikimedia Commons (CC BY-SA-3.0) Technisch zuiver bismuth / Bron: Materialscientist, Wikimedia Commons (CC BY-SA-3.0)
Technisch zuiver bismuth / Bron: Materialscientist, Wikimedia Commons (CC BY-SA-3.0) Groen-geel mineraal bismiet (Bi2O3).Hardheid 4-5 Mohs / Bron: Publiek domein, Wikimedia Commons (PD)
Groen-geel mineraal bismiet (Bi2O3).Hardheid 4-5 Mohs / Bron: Publiek domein, Wikimedia Commons (PD)Het element
| Naam | Symbool | Atoom nummer | Groep | periode | Blok | Kleur | Reeks | Ontdekking |
|---|---|---|---|---|---|---|---|---|
| Bismuth | Bi | 83 | 15 | 6 | P blok] | Zilver wit | overgangsmetaal | Claude F Geoffroy 1753 |
Chemische eigenschappen van het element
| Atoom massa | Oxidatie staten | Electro negativiteit | atoom straal | ionisatie potentiaal | magnetische ordening | kristal structuur |
|---|---|---|---|---|---|---|
| 209 u | 12345 | 2,0 eV Pauling | 156 pm | 1e 703 KJ/mol 2e 1610 KJ/mol 3e 2466KJ/mol | diamagnetisch | rhombohedrisch |
Fysische eigenschappen van het element
| Aggregatie toestand 20 °C | dichtheid g/cm3 | Smelt punt | kook punt | Warmte KJ/mol | Electrische weerstand | Liniaire uitzettings coefficient | thermische geleid- baarheid | Elastici- teits modules | Hard heid |
|---|---|---|---|---|---|---|---|---|---|
| Vast | Vast =9,8 Vloeibaar =10,1 | 271 °C | 1564 °C | smelt =11 verdamping =151 | 130.10-8 Ω.m= =1,3μ.Ω.m | 13,4. 10-6/ °C | 8 W/ °C | 32000 N/mm2 | 2,5 Mohs |
Onder normale omstandigheden kristalliseert bismut in een rhombohedrisch rooster. Wanneer samengeperst bij kamertemperatuur, verandert deze Bi-I structuur eerst in het monokliene Bi-II op 2.55 GPa, en vervolgens in het tetragonale Bi-III op 2,7 GPa en uiteindelijk in een body-centered cubic Bi-IV op 7,7 GPa.
Voorkomen ertsen
Belangrijkste ertsen van bismut zijn bismuthimiet en bismiet. Bismuth komt ook als technisch zuiver metaal voor en wordt gevonden als kristallen in sulfide-ertsen van nikkel, kobalt, zilver en tin. Bismut is meestal een bijproduct van lood en koper winning. De belangrijkste gebieden waar het wordt gewonnen zijn Bolivia, Peru, Japan, Mexico en Canada.Winning van bismuth
- Het metaal dat als element voorkomt is vrij zuiver. De verontreinigingen kunnen verwijderd worden door gesmolten bismuth over een schuine stalen plaat te laten vloeien waardoor de verontreinigingen oxideren en een 'afschepbare' slak vormen.
- Komt ook voor als Bi2S3 (bismuthglans) die door roosten overgaat in bismuthoxide Bi2O3 waaruit het element Bismuth vrij gemaakt wordt door reductie met koolstof.
- Belangrijke bismuth ertsen zijn bismite (Bi 2 O 3), bismuthinite (Bi 2 S 3) en bismutite [(BiO) 2 CO 3]. Bismuth komt hieruit vrij door een reductie van de oxiden met koolstof.
- Recycling van bismut is moeilijk, waarschijnlijk ondoenlijk door de verstrooiing in zeer kleine porties over talrijke toepassing.
Kenmerkende eigenschappen van bismuth
- Geen andere metaal met meer natuurlijk diamagnetisch dan bismuth.
- Bismuth heeft een zeer lage thermische geleidbaarheid bij een zeer hoge elektrische weerstand.
- Bismut is stabiel bij normale temperaturen. Verhit reageert het met water tot bismuth(III)oxide..
- 2 Bi + 3H2O → Bi2O3 + 3H2
- Elementair bismuth heeft de bijzondere eigenschap dat de vloeibare fase dichter is dan de vaste fase. Bismuth dijt 3.32% uit bij stollen, daarom wordt het o.a. gebruikt als laagsmeltende legering voor loden letters in de klassieke drukkerij. het gietstuk wordt nagedrukt en heeft een scherpe vorm. Bismuth kan als legeringselement door zijn uitzetting bij stollen de contractie van de andere elementen compenseren zoals bij bismuth - lood legeringen in een letterzetterij.
Richtprijzen van bismuth
De prijs van Technisch zuiver bismuth schommelt in 2013 tussen 17,5$/kg en 20$/kg. De prijs was Circa 5,00 $ / kg na de oorlog tot circa 1965, daarna zijn de prijzen sterk gestegen met grote schommelingen.Toepassingen van bismuth
- In de VS werd in 2010 van de circa 1000 ton bismuth 65% besteed aan pigmenten en cosmetica, 25% als legeringselement in de metallurgische industrie en 7% in speciale bismuth legeringen voor soldeer en munitie.
- Bepaalde geneesmiddelen bevatten bismuth, zoals oogdruppels die worden gebruikt tegen infecties; behandelingen voor spijsverteringsproblemen; een isotoop van bismut wordt gebruikt om leukemie te behandelen.
- Bismutoxychloride (BiOCl) wordt gebruikt in cosmetica, pigment in verf voor oogschaduw, haarsprays en nagellak. De kristalvorm bevat lagen atomen die licht chromatisch breken, wat resulteert in een iriserende uiterlijk vergelijkbaar met parelmoer.
- Het verschil in dichtheid tussen lood dichtheid 11.32 g/ cm-3 en bismut (dichtheid 9,78 g/cm3 is relatief klein. Bismuth kan meestal lood vervangen (visserij sinkers en lood voor de sportvissers en als vervanging van loodhagel bij de jacht, bismut-tin legering vertoont zelfde ballistische gedrag.
- Industrie gebruikt bismut-verbindingen als katalysatoren bij de productie van de grondstof voor synthetische vezels en rubbers.
- Bismutverbindingen goed zijn voor ongeveer de helft van de productie van bismut. Ze worden gebruikt in cosmetica, pigmenten, en enkele farmaceutische producten.
- Bismut in BSCCO (bismuth, strontium, calcium, koperoxide), groep van vergelijkbare supergeleidende verbindingen met de hoogste supergeleidende overgangstemperatuur.
- Bismuthsubnitraat wordt gebruikt als verfpigment.
- Bismuth telluride is een halfgeleider. Bi 2Te 3 diodes worden o.a gebruikt in koelkasten, CPU- koelers, en als detectoren in infrarood spectrofotometers.
- Bismutvanadaat is een ondoorzichtige gele pigment in 'olie- en acrylverf. Deze verbinding is een niet-toxisch substituut voor citroengeel pigmenten zoals cadmium en lood sulfiden, strontium, barium, chromaten.
- Ingrediënt in smerende vetten.
- Bismut gebruik in de elektronica als een component van een laag smeltpunt soldeer, als vervanging voor de traditionele tin-lood soldeer. De lage toxiciteit is vooral belangrijk voor soldeer voor gebruik in voedselverwerkende industrie en koperen waterleidingen.
- Voor modellen en mallen wegens de gemakklijke gietbaarheid.
- Bismut wordt ook gebruikt als legeringselement bij de productie van bepaalde staalsoorten w.o. smeedbaar gietijzer.
- Veel bismut legeringen worden gebruikt wegens laag smeltpunt in soldeer, in automatische sprinklers, elektrische zekeringen, in branddetectie-en brandblussystemen, de eutectische Pb22 legering smelt bij 47 ° C.
- Laagsmeltende legeringen, zoals Bi-Cd-Pb-Sn legering die smelt bij 70 ° C, worden gebruikt in auto-en luchtvaartindustrie. Voor buigen van dunwandige buizen volgegoten met de legering om vervorming te voorkomen, de vulling wordt verwijderd in heet water.
- Bismut wordt toegevoegd aan metaal om de verspaanbaarheid te verbeteren omdat het de spanen breekt. Ook hier vervangt het in vele gevallen lood.
- Het krimpen bij stollen van lood en de uitzetting tgv stollen van bismuth compenseren elkaar. Dergelijke legeringen worden gebruikt in precisie gieten, bv in de tandheelkunde.
Bismuth milieu en gezondheid
- Bismut wordt bij normaal gebruik niet als toxisch beschouwd en vormt geen bedreiging voor het milieu. Milieu schade door bismuth is niet bekend, dat is deels te danken aan de lage oplosbaarheid van bismuthverbindingen in water.
- Bismut en zijn verbindingen zijn dus heel wat minder toxisch dan andere zware metalen zoals lood en antimoon. De oplosbaarheid in het bloed is laag en wordt gemakkelijk afgevoerd met de urine.
- Toch kan er door te veel Bismuth inname een bismuth vergiftiging ontstaan. De nieren, lever en blaas kunnen aangedaan worden, soms de huid en ademhalingswegen en er vormt zich een zwarte afzetting op het tandvlees. verder diarree, misselijkheid, hoofdpijn, koorts, slapeloosheid, depressie en reumatische pijn.
© 2013 - 2025 Custor, het auteursrecht van dit artikel ligt bij de infoteur. Zonder toestemming is vermenigvuldiging verboden. Per 2021 gaat InfoNu verder als archief, artikelen worden nog maar beperkt geactualiseerd.
 Fosfor: Het elementFosfor is een scheikundig element met symbool P. Het is een niet-metaal dat in verschillende kleuren kan voorkomen waarv…
Fosfor: Het elementFosfor is een scheikundig element met symbool P. Het is een niet-metaal dat in verschillende kleuren kan voorkomen waarv…
 Selenium: Het elementSelenium is een element die in de natuur in gesteenten en de bodem voorkomt. In zuivere vorm bestaat het als metallisch…
Selenium: Het elementSelenium is een element die in de natuur in gesteenten en de bodem voorkomt. In zuivere vorm bestaat het als metallisch…
 Het element tin: Eigenschappen en toepassingenTin is een buigzaam, kneedbaar zilverachtig-wit metaal, bestand tegen zee- en zoet water. De relatief zachte metalen tin…
Het element tin: Eigenschappen en toepassingenTin is een buigzaam, kneedbaar zilverachtig-wit metaal, bestand tegen zee- en zoet water. De relatief zachte metalen tin…
 Molybdeen: Het elementDe naam molybdeen is afgeleid van molubdaina, het Griekse woord voor lood of op lood gelijkend, vanwege de uiterlijke ov…
Molybdeen: Het elementDe naam molybdeen is afgeleid van molubdaina, het Griekse woord voor lood of op lood gelijkend, vanwege de uiterlijke ov…
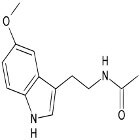 Wat zijn alkaloïden?De term alkaloïden verwijst naar een groep van stoffen of chemische componenten die in planten voorkomen. Alkaloïden beh…
Wat zijn alkaloïden?De term alkaloïden verwijst naar een groep van stoffen of chemische componenten die in planten voorkomen. Alkaloïden beh…
Gerelateerde artikelen
PapierchromatografieChromatografie is de verzamelnaam voor een aantal scheidingstechnieken. Deze technieken berusten allemaal op het princip…
Bronnen en referenties
- http://www.lenntech.com/periodic/elements/bi.htm#ixzz2WOlMNNVY
- http://en.wikipedia.org/wiki/Bismuth
- http://www.metalprices.com/p/BismuthFreeChart
- Leerboek der anorganische chemie Dr A.F. Holleman; JB Wolters Groningen 1953 achttiende druk
- Afbeelding bron 1: Kushboy, Wikimedia Commons (CC BY-SA-3.0)
- Afbeelding bron 2: Materialscientist, Wikimedia Commons (CC BY-SA-3.0)
- Afbeelding bron 3: Publiek domein, Wikimedia Commons (PD)
Custor (173 artikelen)
Laatste update: 13-02-2017
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 7
Laatste update: 13-02-2017
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 7
Per 2021 gaat InfoNu verder als archief. Het grote aanbod van artikelen blijft beschikbaar maar er worden geen nieuwe artikelen meer gepubliceerd en nog maar beperkt geactualiseerd, daardoor kunnen artikelen op bepaalde punten verouderd zijn. Reacties plaatsen bij artikelen is niet meer mogelijk.