Scheidingsmethoden binnen de scheikunde
 In de scheikunde spreken we van een mengsel als een stof meer dan twee soorten deeltjes bevat. Een zuivere stof bestaat helemaal uit dezelfde deeltjes. In de praktijk werken we vaak met mengsels. Zo is melk scheikundig gezien geen zuivere stof, maar een mengsel van water, vetten en meer soorten deeltjes. Zuivere alcohol bestaat voor 96% uit alcohol en 4% uit iets anders, dus dat is scheikundig gezien een mengsel. In dit artikel worden de verschillende manieren besproken om mengsels te scheiden, afhankelijk van de eigenschappen van de stoffen in het mengsel.
In de scheikunde spreken we van een mengsel als een stof meer dan twee soorten deeltjes bevat. Een zuivere stof bestaat helemaal uit dezelfde deeltjes. In de praktijk werken we vaak met mengsels. Zo is melk scheikundig gezien geen zuivere stof, maar een mengsel van water, vetten en meer soorten deeltjes. Zuivere alcohol bestaat voor 96% uit alcohol en 4% uit iets anders, dus dat is scheikundig gezien een mengsel. In dit artikel worden de verschillende manieren besproken om mengsels te scheiden, afhankelijk van de eigenschappen van de stoffen in het mengsel.Extractie
Extractie betekent ‘uittrekking’. Bij extractie maak je gebruik van het verschil in oplosbaarheid tussen stoffen. De bekendste voorbeelden zijn het zetten van koffie en thee. De koffiebonen en theeblaadjes zijn niet oplosbaar in water, maar de geur- en smaakstoffen wel. De actie die je uitvoert, noemen we extraheren.Stel dat je een mengsel hebt van suiker en zout, dan werkt extractie niet. Beide stoffen zijn namelijk goed oplosbaar in water. Wel een goed voorbeeld is kruidenolie en –azijn. Door verschillende kruiden een tijd lang te laten trekken in de olie of azijn, worden de geur- en smaakstoffen van de kruiden overgenomen.
Filtratie
Bij filtratie maak je gebruik van het verschil in deeltjesgrootte. Je kunt het goed vergelijken met zeven, alleen op een kleinere schaal. De deeltjes die in de filter of zeef achterblijven, noemen we residu. Het gefilterde materiaal noemen we filtraat. Deze methode wordt gebruikt om een suspensie te scheiden. Een suspensie is een mengsel van een vloeistof met daarin zwevende vaste deeltjes, zoals sinaasappelsap.Bekende voorbeelden van filtratie zijn een koffiefilter en het scheiden van zand en water. Filtratie kan ook gebruikt worden om lucht te zuiveren van de vaste deeltjes, zoals stof, die in de lucht zitten.
Indampen
Bij indampen worden vaste stoffen, die opgelost zijn in een oplosmiddel, geconcentreerd, door het oplosmiddel te verdampen. Het bekendste voorbeeld is in water opgelost zout. Door het verdampen van water, blijft het zout over. Een ander voorbeeld is het inkoken van jam.Adsorptie
Adsorptie is een scheidingsmethode die berust op verschil in aanhechtingsvermogen. Het meest gebruikte adsorptiemiddel is actieve kool. Dit bestaat dan uit hele kleine deeltjes met een heel groot gezamenlijk oppervlakte. Deeltjes met een groot aanhechtingsvermogen blijven aan de actieve kool hangen. Door vervolgens de actieve kool te filteren, neem je ook de aangehechte stoffen mee. Dit is wat anders dan absorptie (opnemen).Voorbeelden waarbij adsorptie wordt gebruikt zijn waterzuivering, het ontkleuren van oplossingen, het wegvangen van geuren door een afzuigkap en het adsorberen van giftig gas in een gasmasker.
Chromatografie
Er zijn verschillende vormen van chromatografie, om onder andere vloeistoffen en gassen te scheiden. De bekendste vorm van chromatografie vindt plaats met papier. Als met een viltstift een stip op een koffiefilter gezet wordt en de koffiefilter wordt in een laagje water gehouden, gaat de inkt lopen. Deze scheidingsmethode wordt vaak gebruikt om kleurstoffen te onderzoeken.De werking van chromatografie is iets ingewikkelder. Het gaat om het samenspel van een stof met de stationaire fase (het stilstaande materiaal, dus de koffiefilter) en de mobiele fase (het bewegende materiaal, dus het water). Elke kleurstof hecht zich op een andere manier aan de stationaire en mobiele fase, waardoor de kleurstoffen uit elkaar worden getrokken.
Samenvatting
| Scheidingsmethode | Maakt gebruik van | Voorbeeld |
|---|---|---|
| Extractie | Verschil in oplosbaarheid | Koffie zetten |
| Filtratie | Verschil in deeltjesgrootte | Een theezakje |
| Indampen | Verschil in fase | Kalk op een drinkglas |
| Adsorptie | Verschil in aanhechtingsvermogen | Norit |
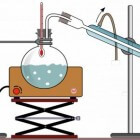
| Destillatie | Verschil in kookpunt | Sterke drank |
| Chromatografie | Verschil in hechting aan de stationaire en mobiele fase | Een koffiefilter met inktvlek in een laagje water houden |