Polymerisatiereacties - Polyadditie en polycondensatie
 Een overeenkomst tussen een boterhamzakje en het toetsenbord is dat ze allebei gemaakt zijn van plastic, maar ze verschillen op het gebied dat een boterhamzakje gemakkelijk vervormd kan worden bij een kleine hoeveelheid verhitting, terwijl het plastic van het toetsenbord onbuigbaar is en ontleedt bij verhitting. Dit heeft te maken met de verschillende productieprocessen. Waarom zijn sommige plastics hard, en andere vervormbaar?
Een overeenkomst tussen een boterhamzakje en het toetsenbord is dat ze allebei gemaakt zijn van plastic, maar ze verschillen op het gebied dat een boterhamzakje gemakkelijk vervormd kan worden bij een kleine hoeveelheid verhitting, terwijl het plastic van het toetsenbord onbuigbaar is en ontleedt bij verhitting. Dit heeft te maken met de verschillende productieprocessen. Waarom zijn sommige plastics hard, en andere vervormbaar?
Soorten reacties
Een polymerisatiereactie is in het dagelijks leven niet meer weg te werken; zowel de industrie als levende wezens voeren dagelijks polymerisatiereacties uit. De reactieproducten die gebruikt kunnen worden variëren van simpele alkenen en alkynen (koolwaterstoffen met dubbele en driedubbele bindingen) tot aminozuren en sacchariden waarmee verschillende eindproducten kunnen worden gemaakt. Tot de polymerisatiereacties behoren twee soorten reacties:- Additiepolymerisatie (polyadditie)
- Condensatiepolymerisatie (polycondensatie)
Additiepolymerisatie
Bij een additiepolymerisatie, ook wel polyadditie genoemd, is er altijd sprake van een alkaan of een alkyn die in drie stappen reageert tot de vorming van een polymeer. Tot deze stappen behoren de initiatie, propagatie en de terminatie. Een voordeel van een additiepolymerisatie is dat er geen stoffen worden afgescheiden tijdens de reactie: het complete product wordt gebruikt.Initiatie
Om een alkeen of alkyn te laten reageren met een ander molecuul (vaak van dezelfde soort) moet de dubbele of driedubbele binding worden opgebroken tot een enkele of dubbele binding waardoor een radicaal ontstaat. Radicalen zijn erg reactief en zullen daarom snel met een atoom of molecuul binden. De initiatie van de polymerisatiereactie van etheen kan dan als volgt uitgedrukt worden, waarbij de initiator, het radicaal, met R is aangegeven:R + H2C=CH2 → R-H2C-CH2
Propagatie
Na de initiatie van de polymerisatiereactie van etheen bevindt de reactie zich in de propagatie-fase. Tijdens de propagatie zal de R-CH2-CH2 verder reageren met andere, in dit geval, etheenmoleculen om zo polyethyleen te vormen. Dit proces kan, afhankelijk van de aanwezige hoeveelheid etheen, leiden tot zeer lange polymeren. De snelheid waarmee de polymerisatie plaatsvindt is afhankelijk van de hoeveelheid etheen die aanwezig is, alsmede in welke concentratie en hoeveel andere initiatoren aanwezig zijn. De propagatie van de polymerisatiereactie van etheen kan als volgt worden uitgedrukt, met de initiatie achterwege gelaten:R + n H2C=CH2 → R-[CH2-CH2](n-1)-H2C-CH2
Terminatie
Om een additiepolymerisatie te stoppen is niet veel nodig. Omdat het uiteinde van het polymeer tijdens de propagatie wordt gelinkt met andere moleculen via een radicaal, is het enige wat nodig is om deze reactie stoppen ook een radicaal. Zo is het mogelijk voor de polymeren om, in plaats van met een ander etheenmolecuul, een reactie aan te gaan met een ander polymeer, mits de productie daarvan nog niet is beëindigd. Immers, als twee radicalen met elkaar binden is de reactie voorbij. Deze reactie wordt als volgt beschreven:2 R-[CH2-CH2](n-1)-CH2-CH2 →R-[CH2-CH2](2n+1)-R
Na de koppeling van twee radicalen is de reactie afgelopen en kan het polymeer verder worden behandeld.
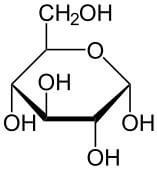 Figuur 1: glucose / Bron: NEUROtiker, Wikimedia Commons (Publiek domein)
Figuur 1: glucose / Bron: NEUROtiker, Wikimedia Commons (Publiek domein)Condensatiepolymerisatie
Een condensatiepolymerisatie, ook wel polycondensatie genoemd, is een polymerisatiereactie waarbij na het binden van twee grotere moleculen een kleiner molecuul wordt afgescheiden. Een condensatiepolymerisatie komt voor bij het maken van suikers, cellulose, eiwitten en alcoholen. Een tegenovergestelde van een een condensatiepolymerisatie is een hydrolyse, waarbij individuele monomeren weer worden bevrijd van hun gebonden staat. Als glucose (C6H12O6) polymeriseert tot saccharose (C12H22O11) scheidt deze reactie water af. In figuur 1 is glucose te zien. Bij een condensatiereactie zal van een glucosemolecuul, of een ander monomeer de complete OH-groep van de 4e koolstof (compleet rechts) of de 6e koolstof (CH2OH-groep) verdwijnen, waarbij bij een ander molecuul alleen de H van de OH-groep zal worden weggehaald. Bij een carbonzuur en een amide zal het carbonzuur zijn OH-groep afstaan die met een H van de NH2-groep van een amide een watermolecuul zal vormen. Dit is een reactie die vooral voorkomt in het menselijk lichaam bij de aanmaak van eiwitten.Eigenschappen van polymeren
Polymeren kunnen bepaalde eigenschappen aannemen. dit is compleet afhankelijk van het monomeer of de monomeren die zijn gebruikt bij het vervaardigen van het polymeer. Dit zijn:- Cross-linking
- Aanwezigheid van functionele groepen
Cross-linking
Cross-linking kan zich alleen voordoen als in het polymeer nog dubbele bindingen aanwezig zijn en er een radicaal wordt toegevoegd aan het polymeer. De dubbele binding zal opbreken en, indien er nog moleculen aanwezig zijn, verder polymeriseren. Indien er wordt gepolymeriseerd met andere polymeren zullen gecrosslinkte structuren ontstaan, waardoor een polymeer van een thermoplast naar een thermoharder kan gaan. Het verschil tussen een thermoplast en een thermoharder is dat een thermoplast vervormd kan worden bij verhitting, terwijl een thermoharder zal ontleden en stinken bij verhitting. Thermoharders zijn, door de gecrosslinkte structuur, ook veel steviger dan een thermoplast.Aanwezigheid van functionele groepen
De aanwezigheid van functionele groepen, zoals een alcohol of een keton, kan het polymeer de mogelijkheid geven om waterstofbruggen te slaan. Dit houdt niet per definitie in dat een polymeer makkelijk zal oplossen, maar dat het polymeer een hydrofiel oppervlakte heeft. Hierdoor wordt water vastgehouden en stroomt het ook niet gemakkelijk af van het polymeer. Indien het alcohol of het keton wordt vervangen door een halogeen, zoals fluor, kan een oppervlak zeer hydrofobisch worden. Dit is het geval met flessen die zijn gemaakt van PTFE (polytetrafluoretheen). Water zal zich niet gemakkelijk aan het oppervlak hechten en stroomt vrijwel direct naar de bodem van de fles. Dit principe wordt ook gebruikt bij de coating van boten: een hydrofobisch oppervlak vaart makkelijker door het water wat brandstof bespaart. De eigenschappen van een polymeer hangen dus af van de monomeren die zijn gebruikt.© 2017 - 2025 Dysprosium, het auteursrecht van dit artikel ligt bij de infoteur. Zonder toestemming is vermenigvuldiging verboden. Per 2021 gaat InfoNu verder als archief, artikelen worden nog maar beperkt geactualiseerd.
 Polymeren en polymerisatieEen polymeer is een keten van zichzelf herhalende moleculen. De moleculen die steeds herhaald worden en dus de basis vor…
Polymeren en polymerisatieEen polymeer is een keten van zichzelf herhalende moleculen. De moleculen die steeds herhaald worden en dus de basis vor…
 Redoxreacties - theorie en berekeningLithium reageert vijandig met water, waarbij waterstofgas en een oplossing van lithiumhydroxide wordt gevormd. Cesium re…
Redoxreacties - theorie en berekeningLithium reageert vijandig met water, waarbij waterstofgas en een oplossing van lithiumhydroxide wordt gevormd. Cesium re…
 Zouten en moleculaire bindingen - soortenIn de scheikunde zijn verschillende bindingen aanwezig tussen moleculen. Deze bindingen zorgen ervoor dat suiker oplost…
Zouten en moleculaire bindingen - soortenIn de scheikunde zijn verschillende bindingen aanwezig tussen moleculen. Deze bindingen zorgen ervoor dat suiker oplost…
Gerelateerde artikelen
Silicium, botten en bindweefselSilicium is het tweede meest voorkomende element in de aardkorst, na zuurstof. Zijn functie in het lichaam is minder nad…
Bronnen en referenties
- Inleidingsfoto: Hans, Pixabay
- Afbeelding bron 1: NEUROtiker, Wikimedia Commons (Publiek domein)
Dysprosium (40 artikelen)
Laatste update: 17-03-2018
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Laatste update: 17-03-2018
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Per 2021 gaat InfoNu verder als archief. Het grote aanbod van artikelen blijft beschikbaar maar er worden geen nieuwe artikelen meer gepubliceerd en nog maar beperkt geactualiseerd, daardoor kunnen artikelen op bepaalde punten verouderd zijn. Reacties plaatsen bij artikelen is niet meer mogelijk.