Xenon: Het element
 Xenon, (van Grieks Xenos is vreemdeling), is een inert edelgas niet-toxisch en chemisch inert. Het is kleurloos, reukloos en smaakloos. Met minder dan 100 deeltjes per miljard is Xenon één van de zeldzaamste natuurlijke elementen in onze atmosfeer. Door Sir William Ramsay en Morris Travers is Xenon ontdekt in het residu dat achterblijft na verdampen van vloeibaar lucht. Het toepassingsgebied van Xenon is zeer breed van autokoplampen tot ionenmotor in ruimtevaartuigen.
Xenon, (van Grieks Xenos is vreemdeling), is een inert edelgas niet-toxisch en chemisch inert. Het is kleurloos, reukloos en smaakloos. Met minder dan 100 deeltjes per miljard is Xenon één van de zeldzaamste natuurlijke elementen in onze atmosfeer. Door Sir William Ramsay en Morris Travers is Xenon ontdekt in het residu dat achterblijft na verdampen van vloeibaar lucht. Het toepassingsgebied van Xenon is zeer breed van autokoplampen tot ionenmotor in ruimtevaartuigen.Plaats van het element Xenon in het periodiek systeem
| Naam | Symbool | Atoomnummer | Groep | Periode | Blok | Reeks | Kleur |
|---|---|---|---|---|---|---|---|
| Xenon | Xe | 54 | Edelgassen:
| Periode 5 | P-blok | Edelgassen | Kleurloos |
Chemische eigenschappen van het element Xenon
| Atoommassa (u) | elektronenconfiguratie | Oxidatietoestanden | Elektronegativiteit (Pauling) | Atoomstraal (pm) | ionisatiepotentiaal (kJ•mol−1) |
|---|---|---|---|---|---|
| 131 | [Kr]4d10 5s2 5p6 | 0 | 2.6 | 131 | 1e 1170 2e 2047 3e 3099 |
Fysische eigenschappen van het element Xenon
| Dichtheid (kg/m3) | Smelt- punt (K) | Kook- punt(K) | Smelt- warmte (kJ•mol−1) | Verdampings- warmte (kJ•mol−1) | Kristal- structuur | Specifieke warmte (J/kg.K) | Warmte geleiding (W/m.K) |
|---|---|---|---|---|---|---|---|
| 5,9 | 161 | 165 | 2,3 | 12,6 | Kubisch | 158 | 0,0056 |
 Bron: Alchemist-hp (www.pse-mendelejew.de), Wikimedia Commons (FAL)
Bron: Alchemist-hp (www.pse-mendelejew.de), Wikimedia Commons (FAL)Toepassingen van Xenon
Het gas Xenon wordt gebruikt in diverse Xenonlampen, zoals bacteriële lampen, elektronenbuizen, stroboscopen, elektronenflitsers, in robijnlasers. Het licht van xenon wordt gebruikt als biocide en wordt als laser gebruikt. Xenon produceert een scherpe witte lichtflits wanneer er elektrische spanning op wordt gezet en wordt daarom aangewend in stroboscooplampen.Xenon als doping
Xenon in kleine hoeveelheden ingeademd, werkt prestatiebevorderend. Volgens onderzoekers stijgt bij dierproeven met Xenongas de productie van rode bloedlichaampjes met 60 procent. Xenon gas in kleine hoeveelheden gecontroleerd ingeademd stimuleert de productie van rode bloedlichaampjes. Na de Olympische Winterspelen van 2014 kwamen er berichten dat Rusland het middel al 10 jaar in de sport toepast. De edelgassen Xenon en Argon staan heden op de lijst van verboden middelen in de sport.
Xenon in de OK
De isotoop 133Xe wordt gebruikt als radio-isotoop. Xenon wordt gebruikt in de anesthesie. Het gas is relatief veilig voor het hart.
Britse artsen hebben hersenletsel bij een zuigeling voorkomen door de hersens te koelen met Xenon. Het werd geboren zonder zelf te kunnen ademen en zijn hartslag was instabiel. De hersens toonden tekenen van naderende letsel door zuurstof gebrek. De artsen hebben zijn vermogen te ademen hersteld en zijn hartritme gestabiliseerd, in tussentijd hebben ze de hersens gekoeld met Xenon. Testen hadden aangetoond dat koeling met Xenon de hersens beschadiging vertragen bij zuurstof gebrek.
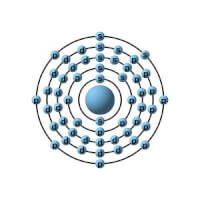 Bron: Peo at da.wikipedia, Wikimedia Commons (CC BY-SA-3.0)
Bron: Peo at da.wikipedia, Wikimedia Commons (CC BY-SA-3.0)Xenon beschikt als andere edelgassen over een geheel gevulde buitenste elektronenschil waardoor er geen drang is tot reacties met andere elementen en dus geen verbindingen met andere elementen zou moeten vormen. Toch zijn er omstandigheden waarbij Xenon reacties aangaat met andere elementen. Naast fluorideverbindingen zoals Xenondi-, tetra- en hexafluoride (XeF2, XeF4 en XeF6) bestaan en het zeer explosieve Xenontrioxide (XeO3) en Xenontetraoxide (XeO4). Hierbij neemt Xenon 2, 4, 6 of 8 elektronen op. Later zijn meer verbindingen tot stand gekomen zoals: Xenonhydraat (Xe(H2O)n), waarbij n = 5 of 6, Xenonplatinumhexafluoride (XePtF6), en Xenonrhodiumhexafluoride (XeRhF6).
Xeon autokoplampen
HID (High Intensity Discharge), verwijst naar lampen gevuld met Xenon gas, in plaats van de gangbare gloeilampen. Het gas ontbrandt bij blootstelling aan hoge elektrische spanning. de HID xenon lichten produceren bijna drie keer meer licht dan de standaard lampen. Het xenon gas verandert de lichtkleur afhankelijk van de temperatuur. Hoe groter de temperatuur, hoe duidelijker helderder witter het geproduceerde licht.
Xenon ionen worden gebruikt als brandstof in een ionenmotor aan boord van het ruimteschip Deep Space 1.
Voorkomen van xenon
In de atmosfeer komt Xenon sporadisch voor. Op commerciële basis wordt het verkregen door extractie van vloeibare lucht.133Xe en 135Xe worden in atoomreactoren aangemaakt.
De meest stabiele isotopen van het element xenon
| Isotoop | RA(%) | Halveringstijd | Verval | VE(MeV) | Vervalproduct |
|---|---|---|---|---|---|
| 124Xe | 0,10 | 10^17 jaar | 2EV | 8,8 | 124Te |
| 125Xe | Synthetisch | 16,9 uur | EV | 1,65 | 125i |
| 126Xe | 0,09 | Stabiel met 72 neutronen | --- | --- | --- |
| 127Xe | Synthetisch | 36,4 dag | EV | 0,66 | 127i |
| 128Xe | 1,91 | Stabiel met 74 neutronen | --- | --- | --- |
| 129Xe | 26,4 | Stabiel met 75 neutronen | --- | --- | --- |
| 130Xe | 4,1 | Stabiel met 76 neutronen | --- | --- | --- |
| 131Xe | 21,2 | stabiel met 77 neutronen | --- | --- | --- |
| 132Xe | 26,9 | Stabiel met 78 neutronen | --- | --- | --- |
| 133Xe | Synthetisch | 5,25 dag | beta | 0,43 | 133Cs |
| 134Xe | 10,4 | Stabiel met 80 neutronen | --- | --- | --- |
| 135Xe | Synthetisch | 9,14 uur | beta | 1,15 | 135Cs |
| 136Xe | 8,9 | 9,3.10^19 jaar | 2 beta | 7,6 | 136Ba |
Milieu en gezondheid in relatie tot Xenon
Xenon zelf is niet giftig maar veel Xenon verbindingen zijn dat wel door de sterke oxiderende werking. Er zijn geen ecologische schade op de lange termijn waargenomen. Xenon is niet kankerverwekkendHet effect van inerte niet giftige doch verstikkende gassen wordt bepaald door de hoeveelheid zuurstof die verdrongen wordt door xenon. De symptomen bij toenemend gebrek aan zuurstof zijn: kortademigheid, hyperventilatie, minder alert, afnemende spiercoördinatie, zintuigen werken slechter, emotioneel instabiel, snel moe, misselijkheid, braken, hoofdpijn, bewusteloosheid, krampen, coma en tenslotte overlijden.