Helium: Het element
 Helium werd in 1868 door de Fransman Pierre Janssen en de Engelsman Norman Lockyer ontdekt in het licht van de zon tijdens een zonsverduistering, ze zagen in hun spectroscoop een emissielijn van een onbekend element dat we nu kennen als helium. In 1895 lukte het de Nederlander Kamerling Onnes om helium vloeibaar te maken en In 1907 toonde Ernest Rutherford aan dat alfadeeltjes uit radioactieve straling heliumkernen zijn. Helium is een kleurloos en reukloos edelgas met de laagste kookpunt (4,2 kelvin) van alle elementen. Na waterstof is het, het meest voorkomende element in het universum.
Helium werd in 1868 door de Fransman Pierre Janssen en de Engelsman Norman Lockyer ontdekt in het licht van de zon tijdens een zonsverduistering, ze zagen in hun spectroscoop een emissielijn van een onbekend element dat we nu kennen als helium. In 1895 lukte het de Nederlander Kamerling Onnes om helium vloeibaar te maken en In 1907 toonde Ernest Rutherford aan dat alfadeeltjes uit radioactieve straling heliumkernen zijn. Helium is een kleurloos en reukloos edelgas met de laagste kookpunt (4,2 kelvin) van alle elementen. Na waterstof is het, het meest voorkomende element in het universum.Plaats helium in het periodiek systeem
| Naam | Symbool | Atoomnummer | Groep | Periode | Blok | Reeks | Kleur |
|---|---|---|---|---|---|---|---|
| Helium | He | 2 |
| Periode 1 | S-blok | Edelgassen | Kleurloos |
Chemische eigenschappen van helium
| Atoommassa (u) | Elektronenconfiguratie | Oxidatietoestanden | Atoomstraal (pm) | ionisatiepotentiaal (kJ•mol−1) |
|---|---|---|---|---|
| 4,0 | 1s2 | 0 | 31 | 1e 2372 2e 5251 |
Fysische eigenschappen van helium
| Dicht- heid (kg•m−3) | Kook- punt (K) | Verdampings- warmte (kJ/mol) | Van der Waals straal (pm) | Molair volume (m3/mol) | Geluids- snelheid (m/s) | Specifieke warmte (J/kg.K) | Warmte- geleiding (W/m.K) |
|---|---|---|---|---|---|---|---|
| 0,1787 | 4,2 | 0,0845 | 140 | 32,07 (vloeibaar) | 970 | 5193 | 0,1513 |
Stabielste helium Isotopen
| naam | Protonen | neutronen | halveringstijd |
|---|---|---|---|
| 3He | 2 | 1 | stabiel |
| 4He | 2 | 2 | stabiel |
 Periodiek systeem van elementen / Bron: Cepheus, Wikimedia Commons (Publiek domein)
Periodiek systeem van elementen / Bron: Cepheus, Wikimedia Commons (Publiek domein)Gebruikseigenschappen
De helium isotopen 4He en 3He zijn gevormd tijdens de Oerknal. De stabiele heliumisotoop 4He komt het meest voor. De kern bestaat uit twee protonen en twee neutronen. Zwaardere kernen vervallen door alfaverval d.w.z. door uitzending van een 4He-kern, (alfadeeltjes zijn namelijk heliumkernen). Een tweede heliumisotoop, 3He, heeft 1 neutron en komt op Aarde relatief weinig voor. De verhouding tussen de twee isotopen (3He/4He) gemeten in de zonnewind is circa 4 keer hoger dan in meteorieten en 300 keer hoger dan in de aardatmosfeer.De verhouding 3He/4He wordt gebruikt om de oorsprong van lava en magma van vulkanen te bepalen. De kritische temperatuur van Helium is slechts 5,19 K.
Helium stolt tot vaste fase alleen onder hoge druk, onder atmosferische druk gebeurt dat niet, slechts bij temperaturen van circa 1K stolt helium bij een druk van circa 2,6 MPa (260 N/cm2) en bij kamertemperatuur bij een druk van 20 GPa. (2.10↑6 N/cm↑2)
Helium is een edelgas en chemisch inert, maar beschoten met elektronen (d.i. bétastraling) vormt het negatieve ionen die toch verbindingen kunnen aangaan met sommige andere elementen.
Helium lost slecht op in water.
Toepassingen
Neonbuizen. Neon is de algemene benaming, in de praktijk worden meerdere gassen gebruikt om even zovele kleuren te realiseren.- Helium wordt gebruikt als beschermgas bij elektrisch booglassen en als beschermgas waarin silicium- en germanium kristallen moeten groeien.
- In gasontladingslampen (neonbuizen).
- Vanwege het zeer kleine atoommolecuul wordt helium gebruikt om de dichtheid van vaten en leidingen te testen. Een ruimte wordt gevuld met helium en met een detector worden de ontsnapte helium atomen geteld. als er geen helium atomen ontsnappen ontsnapt geen enkel ander atoom.
- Bij raketten wordt helium gebruikt om de ruimte in brandstoftanks te vullen die ontstaat door brandstofverbruik.
Luchtschepen
Helium is lichter dan lucht en wordt gebruikt als vulmiddel in ballonnen en luchtschepen. De stijgkracht van helium is circa 90% van die van waterstof, maar waterstof is berucht om zijn brandbaarheid.
Koelmiddel
Helium is zeer geschikt voor koeling van systemen tot lage temperaturen zoals supergeleidende magneten en cryogene toepassing. Vloeibare helium wordt gebruikt bij MRI-scans als koeling voor supergeleidende elektromagneten.
Duikers
Zuurstof en stikstof veroorzaken bij hoge waterdruk lichamelijke problemen zoals stikstofnarcose en caissonziekte. Zuurstof en stikstof worden daarom deels vervangen door helium. Helium verlaagt de inwendige wrijving van het mengsel waardoor het in en uitademen gemakkelijker wordt.
Helium gevulde Hard-Disk Drives (HDD's)
Afdichten van de schijvenruimte in HDD’s met helium is moeilijk wegens de zeer kleine afmeting van het atoom zodat voorkomen van lekkage een technische uitdaging bleek. De met helium gevulde HDD ruimte vermindert de weerstand, het lawaai, de temperatuur en de energie nodig voor de aandrijving van de schijven. Met behulp van helium in plaats van lucht in HDD's vermindert turbulentie en trilling. De nauwkeurigheid van het systeem is groter omdat de spoor-mis registratie wordt verminderd. Schijven worden dunner dus zijn er extra schijven in het station mogelijk en kunnen de gegevens-tracks dichter bij elkaar worden geplaatst. Bovendien kunnen de met helium gevulde schijvenruim veel hogere snelheden gerealiseerd worden, waardoor de toegangstijd tot de gegevens verkort met circa 25%.
 Luchtschepen worden gevuld met het niet brandbare helium / Bron: Derek Jensen (Tysto), Wikimedia Commons (Publiek domein)
Luchtschepen worden gevuld met het niet brandbare helium / Bron: Derek Jensen (Tysto), Wikimedia Commons (Publiek domein) Helium in een neonbuis / Bron: Alchemist-hp (www.pse-mendelejew.de), Wikimedia Commons (GFDL-1.2)
Helium in een neonbuis / Bron: Alchemist-hp (www.pse-mendelejew.de), Wikimedia Commons (GFDL-1.2)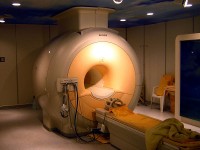 MRI scan wordt gekoeld met vloeibaar helium / Bron: KasugaHuang, Wikimedia Commons (CC BY-SA-3.0)
MRI scan wordt gekoeld met vloeibaar helium / Bron: KasugaHuang, Wikimedia Commons (CC BY-SA-3.0)