Zwavel: Het element
 Zwavel wordt gebruikt voor de bereiding van zwavelzuur, voor het vulkaniseren van rubber, voor plantenziekte bestrijding, voor de luciferfabricage, voor de bereiding van zwavelkoolstof en voor zwavelverbindingen. Circa 3% van de massa van de aarde is zwavel, een hoeveelheid waarvan twee manen “gekleid” kunnen worden. Het is een essentieel element voor levende organismen dat zich onder meer bevindt in bepaalde amino-zuren.
Zwavel wordt gebruikt voor de bereiding van zwavelzuur, voor het vulkaniseren van rubber, voor plantenziekte bestrijding, voor de luciferfabricage, voor de bereiding van zwavelkoolstof en voor zwavelverbindingen. Circa 3% van de massa van de aarde is zwavel, een hoeveelheid waarvan twee manen “gekleid” kunnen worden. Het is een essentieel element voor levende organismen dat zich onder meer bevindt in bepaalde amino-zuren. Bron: Kushboy, Wikimedia Commons (CC BY-SA-3.0)
Bron: Kushboy, Wikimedia Commons (CC BY-SA-3.0)Plaats van zwavel in het periodiek systeem
Zwavel is een scheikundig element met het symbool S en atoomnummer 16. Het is een meerwaardige niet-metaal. Elementaire zwavel is een helder gele kristallijne vaste stof bij kamertemperatuur. Zwavel brandt met een blauwe vlam gelijktijdig met de vorming van zwaveldioxide, opmerkelijk is de verstikkende geur.Algemene eigenschappen van zwavel
| Naam | Symbool | Atoomnummer | Groep | periode | Blok | Reeks | Kleur |
|---|---|---|---|---|---|---|---|
| Zwavel Sulfur | S | 16 | groep 16? | Periode 3 | P-blok | polyatomisch niet metaal | citroengeel gesinterd microkristallen |
Chemische eigenschappen van zwavel
| Atoommassa (u) | Elektronen- configuratie | Oxidatie- toestanden | Elektro- negativiteit (Pauling) | Atoom- straal | ionisatie- potentiaal (kJ/mol) |
|---|---|---|---|---|---|
| 32,06 | per shell:2, 8, 6 [Ne] 3s2 3p4 | 6, 5, 4, 3, 2, 1, −1, −2 (sterke zure oxide) | 2.58 | Covalent radius: 105±3 pm v/d Waals radius: 180 pm | 1e: 999.6 2e: 2252 3e: 3357 |
Fysische eigenschappen van zwavel
| Dicht heid (g/cm3) | Smelt- punt (K) | Kook- punt (K) | Aggregatie- toestand resp magnetische ordening | Smelt- warmte (KJ/mol) | Verdamp- ings- warmte (KJ/mol) | Kristal- structuur Resp. Hardheid | Elek- trische weerstand (Ω•m | Warmte- geleiding (W/m.K) |
|---|---|---|---|---|---|---|---|---|
| Alpha: 2.07 Beta: 1.96 Gamma: 1.92 | 288,40 | 718,80 | Vast resp. Dia- magnetisch | 1.727 | 45 | Ortho- rombisch resp 2 Mohs | 2x10↑15 (amorf)) | 0.205 (amorf) |
Isotopen
Zwavel is 25 bekend isotopen, waarvan vier stabiele 32S (95.02%), 33S (0,75%), 34S (4,21%) en 36S (0,02%). Anders dan 35S, met een halfwaardetijd van 87 dagen en gevormd kosmische stralen spallation van 40Ar, de radioactieve isotopen van zwavel halveringstijd van minder dan 3 uur.De stabielste isotopen
| Isotoop | NA(%) | Halveringstijd | Verval via | Vervalenergie | Vervalproducten |
|---|---|---|---|---|---|
| 32S | 95 | Stabiel met 16 neutronen | [/TD][TD] | [/TD] | |
| 0,75 | Stabiel met 17 neutronen | [/TD][TD] | [/TD] | ||
| 4,20 | Stabiel met 18 neutronen | [/TD][TD] | [/TD] | ||
| Synthetisch | 87,30 dagen | Beta- | 0,167 | 35Cl | |
| 36S | 0,02 | Stabiel met 20 neutronen | [/TD][TD] | [TD][/TD]
Kenmerkende eigenschappen
- Onder normale omstandigheden, vormen zwavel atomen cyclische octatomic moleculen met chemische formule S8.
- Chemisch kan zwavel reageren als oxidant en als reductie middel. Het oxideert meeste metalen en verscheidene niet-metalen, inclusief koolstof.
- Waterstofsulfide (H2S) heeft de geur van rotte eieren.
- Zwavel brandt met een blauwe vlam onder vorming van zwaveldioxide (SO2).
- Zwavel is onoplosbaar in water maar goed oplosbaar in koolstofdisulfide, in mindere mate in andere organische oplosmiddelen, zoals tolueen en benzeen.
- In water opgelost is waterstofsulfide een zwak zuur: H2S↔ HS- + H+ .
- Waterstofsulfide gas en waterstofsulfide anionen zijn zeer giftig voor zoogdieren, wegens vermindering van het zuurstof-dragend vermogen van hemoglobine, zoals ook wordt veroorzaakt door het bekendere gif cyanide.
- Reductie van elementaire zwavel geeft polysulfiden, die bestaan uit ketens van zwavelatomen: 2 Na + S8 → Na2S8.
- Meest kenmerkende eigenschap van zwavel is het vermogen om zich koppelen (zich te binden) door vorming van ketens, S8 is een keten van 8 zwavelatomen.
- De radicale anion S3- geeft de blauwe kleur aan het mineraal lapis lazuli (lazuursteen) een azuurblauwe ondoorzichtig gesteente waarin de belangrijkste component is lazuriet (tot 40%).
- De belangrijkste zwaveloxiden worden verkregen door het verbranden van zwavel:
- S + O2 → SO2 en 2 SO2 + O2 → 2 SO3
 Zwavel / Bron: Thomas Bresson, Wikimedia Commons (CC BY-2.5)
Zwavel / Bron: Thomas Bresson, Wikimedia Commons (CC BY-2.5)Het voorkomen van zwavel
- Zwavel komt van nature voor als element, als sulfide en als sulfaat mineralen.
- Elementaire zwavel komt voor in de lava van vulkanen en in hydrothermale bronnen, vooral langs de pacifische ring van vuur.
- In de natuur voorkomende zwavelverbindingen zijn sulfide mineralen, zoals pyriet (ijzersulfide), cinnaber (kwik sulfide), Galena (lood-sulfide), sfaleriet (zinksulfide) en stibniet (antimoon sulfide); en sulfaten, zoals gips (calciumsulfaat), alunite (kalium-aluminium sulfaat) en bariet (bariumsulfaat).
- Tegenwoordig wordt zwavel geproduceerd uit aardolie, aardgas, via hoofdzakelijk waterstofsulfide. De resulterende waterstofsulfide uit dit proces wordt omgezet in elementair zwavel door het Claus-proces. Dit proces omvat oxidatie van waterstofsulfide en zwaveldioxide volgens:
- 3 O2 + 2 H2S → 2 SO2 + 2 H2O en SO2 + 2 H2S → 3 S + 2 H2O
- De wereldproductie van zwavel in 2011 was 70 miljoen ton. Waarvan China 10-, de VS 9-, Canada 7- en Rusland 7 miljoen ton. De rest wordt in circa 15 andere landen geproduceerd. Grootste commercieel gebruik van zwavel (na zwavelzuur) is sulfaat en fosfaat voor kunstmest.
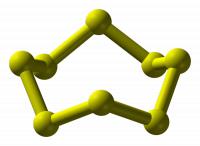 Zwavel atomen hebben de neiging ringen te vormen / Bron: Publiek domein, Wikimedia Commons (PD)
Zwavel atomen hebben de neiging ringen te vormen / Bron: Publiek domein, Wikimedia Commons (PD)Allotropen
Zwavel vormt polyatomic moleculen met verschillende chemische formules, de bekendste allotroop is octasulfur, cyclo-S8. Octasulfur is een zacht, licht-gele vaste stof met de geur van een aangestreken lucifers. Zwavel sublimeert gemakkelijk. Beneden 95 °C bestaat de structuur (cyclo-octasulfur) uit rombische kristallen en boven de 95°C uit monokliene kristallen.Tussen smeltpunt en kookpunt, verandert de atomaire ordening opnieuw, nu van beta octasulfur naar gamma zwavel, vergezeld van verhoogde viscositeit vanwege de vorming van polymeren. Amorfe ("plastische") zwavel wordt geproduceerd door snelle afkoeling van gesmolten zwavel, door gieten in koud water. De lange opgerolde polymere moleculen maken het dan bruinachtige stof elastisch, het voelt als rubber. De vorm is metastabiel en keert bij kamertemperatuur geleidelijk terug naar de moleculaire allotroop. Alle stabiele allotropen zijn elektrische isolatoren.
Verbindingen zwavel en waterstof
Zwavelwaterstof (H2S) komt voor in vulkaangassen, in bodemgassen en het ontstaat door rotting van eiwitten. Het is een kleurloos gas met de geur van rotte eieren. Het is giftig bij inademen. Het kan bereid worden door reactie van bepaalde zuren met bepaalde sulfides; bijvoorbeeld:FeS + H2SO4→ FeSO4 + H2S↑
Zwavelwaterstof (H2S) is brandbaar, bij verbranding vormt zich zwaveldioxide (SO2) en water(H2O):
2H2S + 3O2→ 2SO2 + 2H2O
Zwavelwaterstof is een krachtige reductor, leidt men H2S in de oplossing van ferrizout(FeCl3) dan wordt die tot ferrozout(FeCl2) gereduceerd terwijl de zwavel neerslaat:
2FeCl3 + H2S→ 2FeCl2 + 2HCl + S↓
Zwavelwaterstof opgelost in water gedraagt zich chemisch als een zwak zuur.
Toepassingen van zwavel en zijn verbindingen
- Bekende toepassingen van het element zijn, insecticiden en fungiciden. (Fungiciden zijn bestrijdingsmiddelen ter voorkoming van schimmels op fruit)
- Zwavel is een essentieel element voor alle leven, en veel gebruikt in biochemische processen. Zwavel in organische vorm aanwezig in de vitaminen biotine en thiamine.
- Zwavel is een belangrijk onderdeel van vele enzymen en antioxidant moleculen zoals glutathion en thioredoxine. Organisch gebonden zwavel is onderdeel van alle proteïnen, zoals de amino acids cysteine en methionine. Disulfide verbindingen zijn grotendeels verantwoordelijk voor de sterkte en oplosbaarheid van het eiwit keratine, in haar en veren.
- De normale oxidatie toestanden van zwavel zijn -2 tot +6. Zwavel vormt stabiele verbindingen die een groot toepassingsgebied hebben.
- 16 Na + S8 → 8 Na2S. Deze omzetting gebeurt o.a.in de krachtige natrium-zwavel batterijen.
 Natriumsulfide / Bron: W. Oelen, Wikimedia Commons (CC BY-SA-3.0)
Natriumsulfide / Bron: W. Oelen, Wikimedia Commons (CC BY-SA-3.0) - Verbindingen tussen koolstof en zwavel zijn zeldzaam met de opmerkelijke uitzondering van zwavelkoolstof, een vluchtige kleurloze vloeistof die is structureel vergelijkbaar met kooldioxide. Het wordt gebruikt als een reagens om het polymeer rayon en vele organozwavel verbindingen te maken.
- Organische zwavelverbindingen zijn verantwoordelijk voor enkele van de onaangename geur van rottend organisch materiaal. Ze worden gebruikt als geur toevoeging aan aardgas. Niet alle organische zwavelverbindingen hebben een onaangename geur bij alle concentraties: de zwavelhoudende monoterpenoid grapefruit mercaptan in kleine concentraties is verantwoordelijk voor de kenmerkende geur van grapefruit.
- Bij het vulkaniseren wordt zwavel verwarmd met de rubber tot het punt dat chemische reacties disulfidebruggen vormen tussen isopreen eenheden van het polymeer (polysulfiden verknopen tot polymeren).Dit proces, gepatenteerd in 1843, maakte van rubber een belangrijk product, vooral voor autobanden.
- Gesmolten zwavel wordt soms gebruikt voor het vastzetten van stalen bouten in geboorde gaten in beton waar schokbestendige verbindingspunten wenselijk zijn van apparatuur.
- Pure poedervormige zwavel werd gebruikt als geneesmiddel tonic en laxeermiddel.
- Met de komst van het contact proces wordt de meerderheid van de zwavel tegenwoordig gebruikt om zwavelzuur te maken voor een breed scala van toepassingen, in het bijzonder kunstmest.
- Calcium sulfaat, gips (CaSO4 • 2H2O) wordt gewonnen op de schaal van 100 miljoen ton per jaar voor gebruik in Portland cement en mest.
- Zwavel reageert met methaan tot koolstofdisulfide, dat wordt gebruikt om cellofaan en rayon te vervaardigen.
- Sulfieten worden intensief gebruikt om bleekwater papier en als conserveermiddel in gedroogd fruit.
- Bij de zilver fotografie werden natrium en ammoniumthiosulfaat op grote schaal gebruikt als "fixeermiddelen."
- Zwavel is een bestanddeel van buskruit.
- Organozwavel verbindingen worden gebruikt in geneesmiddelen, kleurstoffen, en landbouwchemicaliën. Veel geneesmiddelen bevatten zwavel, vroege voorbeelden zijn antibacterialsulfonamides zogenaamde sulfa drugs. Zwavel is een onderdeel van vele bacteriële verdediging moleculen. De meeste β-lactam antibiotica, zoals penicillines, cefalosporines and monolactams bevatten zwavel.
- Magnesiumsulfaat, bekend als Epsomzouten als in gehydrateerde kristallijne vorm, kan worden gebruikt als een laxeermiddel, een bad additief, een exfoliant, magnesium supplement voor planten, of als droogmiddel.
Zwavelzuur een indicator voor industriële ontwikkeling
Elementaire zwavel wordt voornamelijk gebruikt als component van zwavelverbindingen. Ongeveer 85% (1989) omgezet in zwavelzuur (H2SO4) volgens het principe: 2 S + 3 O2 + 2 H2O → 2 H2SO4Zwavelzuur is van groot belang voor de wereld economie, het verbruik is een indicator van de industriële ontwikkeling. Bijvoorbeeld met 32,5 miljoen ton in 2010, verbruikt de Verenigde Staten meer zwavelzuur per jaar dan welke ander land per hoofd bevolking. De belangrijkste toepassing van het zuur is de winning van fosfaat ertsen voor mest. Andere toepassingen van zwavelzuur zijn in olieraffinage, afvalwater verwerken, en delfstoffenwinning.
Meststoffen
Zwavel is een bestanddeel van bepaalde meststoffen. De belangrijkste vorm van zwavel is het mineraal calciumsulfaat. Elementaire zwavel is hydrofoob (d.w.z. niet oplosbaar in water), dus niet rechtstreeks op te nemen door planten. Na verloop van tijd converteren bodembacteriën naar in planten oplosbare derivaten.Zwavel verbetert de efficiëntie van andere voedingsstoffen voor planten, zoals stikstof en fosfor. Zwavel te kort in de landbouw komt steeds meer voor in Europa wegens daling van de zwavel (verontreiniging) in de atmosfeer.Het zwaveltekort in de planten zal toenemen, tenzij zwavelhoudende meststof wordt gebruikt.Fungiciden en pesticiden
Elementaire zwavel is een van de oudste en schimmelwerende stoffen. Elementair zwavel in poedervorm, is een veel voorkomende fungicide voor druiven, aardbeien, groenten en vele andere gewassen. Het heeft een goede werkzaamheid tegen een breed scala van ziekten. In de biologische productie is zwavel de belangrijkste fungicide. Biosulfur (biologisch geproduceerd elementaire zwavel met hydrofiele eigenschappen) kan goed worden gebruikt voor deze toepassingen. Elementair zwavel poeder wordt gebruikt als een "organische" insecticide tegen teken en mijten.Cavebacteriën
Cave(grot) bacteriën die waterstofsulfide verteren, produceren "snot" (slijmerige stalactieten in grotten). Deze druppelen zwavelzuur met een pH-waarde zo laag als nul - dat is genoeg om gaten te branden in je kleren. "Snot" bacteriën gedijen in gebieden met zwavel deposito's of zwavelhoudende mineralen of koolwaterstoffen. Het zwavelzuur dat ze uitscheiden vreet in miljoenen jaren nieuwe grottenstelsels ondergronds, door de rotsen op te lossen.Invloed van zwavel op milieu en volksgezondheid
- Waterstofsulfide gas en waterstofsulfide anionen zijn zeer giftig voor zoogdieren, door vermindering van de zuurstof-dragende capaciteit van hemoglobine, zoals ook gebeurt t.g.v. cyanide.
- De verbranding van kolen en/of aardolieproducten door de industrie en energiecentrales genererend zwaveldioxide (SO2), die reageert met vocht en zuurstof en vormt zwavelzuur (H2SO4) en zwaveligzuur (H2SO3). Deze zuren vormen de zure regen, wat leidt tot schade aan het milieu.
- Normen voor brandstoffen vereisen dat zwavel uit fossiele brandstoffen wordt gehaald voor of tijdens verbranding. Dit geëxtraheerd zwavel dekt tegenwoordig een belangrijk deel van de zwavel behoefte.
- Waterstofsulfide is even giftig als waterstofcyanide, maar watersofsulfide is in de praktijk minder gevaarlijk omdat het waarschuwt door de stank. Opgeloste sulfide en hydrosulfide zouten zijn eveneens giftig. In al deze gevallen werkt het gif op dezelfde manier.
Koolstofdisulfide, waterstofsulfide en zwaveldioxide zijn erg giftig.
- Bij 0.03 (ppm) waterstofsulfide kunnen we de gas ruiken maar het is ongevaarlijk bij 8 uur blootstelling.
- Bij 4 (ppm) veroorzaakt waterstofsulfide oogirritatie.
- Bij 20 (ppm) blootstelling aan waterstofsulfide voor meer dan een minuut veroorzaakt het aantasting van oogzenuwen.
- Bij 700 ppm stopt de ademhaling, de dood treedt in als er niet snel medisch hulp komt. Permanent hersenschade kan na reanimatie ontstaan.