Cadmium: het element
 Cadmium werd in 1817 ontdekt door de Duitse chemicus Friedrich Strohmeyer in het mineraal calamiet (zinkcarbonaat). De naam is afkomstig van het Latijnse cadmia, een benaming voor zinkcarbonaat. Cadmium is een bijproduct van de zink- en koperwinning. Het is een giftig zwaar metaal. Van nature komt er jaarlijks 25000 ton cadmium in het milieu terecht, de helft door erosie van gesteenten, de andere helft door bosbranden, vulkaanuitbarstingen en door menselijke handelen.
Cadmium werd in 1817 ontdekt door de Duitse chemicus Friedrich Strohmeyer in het mineraal calamiet (zinkcarbonaat). De naam is afkomstig van het Latijnse cadmia, een benaming voor zinkcarbonaat. Cadmium is een bijproduct van de zink- en koperwinning. Het is een giftig zwaar metaal. Van nature komt er jaarlijks 25000 ton cadmium in het milieu terecht, de helft door erosie van gesteenten, de andere helft door bosbranden, vulkaanuitbarstingen en door menselijke handelen.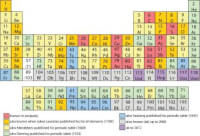 Bron: Sandbh, Wikimedia Commons (CC BY-SA-3.0)
Bron: Sandbh, Wikimedia Commons (CC BY-SA-3.0)Plaats van cadmium in het periodiek systeem
Cadmium behoort tot de toxische zware metalen. Het bevindt zich tussen zink en kwik in kolom 12 van het periodiek systeem. Het is een zacht, blauwachtig wit metaal dat met een mes is te snijden. Interessant is de typische cadmium "scream" bij het buigen van een cadmium staaf, zoals ook bekend is bij tin. Cadmium en zijn verbindingen zijn giftig.| Naam | Symbool | Atoomnummer | Groep | Periode | Blok | Reeks | Kleur |
|---|---|---|---|---|---|---|---|
| Cadmium | Cd | 48 | Zinkgroep Zink Cadmium Kwik Copernicium | 5 | D-blok | overgangsmetalen | zilvergrijs |
Chemische eigenschappen van cadmium
| Atoom- massa(u) | Elektronen- configuratie | Oxidatie- toestanden | Elektro- negativiteit (Pauling) | Atoom- straal(pm) | ionisatie- potentiaal (kJ/mol) |
|---|---|---|---|---|---|
| 112 | [Kr]4d10 5s2 | +2 | 1,69 | 151 | 1e 868 2e 1631 3e 3616 |
Fysische eigenschappen van cadmium
| Dicht- heid (kg/m3) | Hard- heid Mohs | Smelt- punt (K) | Kook- punt (K) | Smelt- warmte (KJ/mol) | Verdamp- ings- warmte (KJ/mol) | Kristal structuur | Geluids- snelheid (m/s) | Speci- fieke warmte (J/kg.K) | Elek- trische weerstand (μΩ.cm) | Warmte- geleiding (W/m.K) |
|---|---|---|---|---|---|---|---|---|---|---|
| 8650 | 2,0 | 594 | 1038 | 6,19 | 99,6 | Hexa- gonaal | 2310 | 230 | 6,8 | 96,8 |
De stabielste isotopen van cadmium
Van nature komen er op aarde zes stabiele cadmiumisotopen voor. Er zijn 27 radio-isotopen, waarvan 113Cd de langste halveringstijd heeft van 7,7x10↑15 jaar en 12% van het totaal aanwezige cadmium uitmaakt. De overige radioactieve isotopen, waaronder 103 cadmium, hebben halveringstijden van minuten tot dagen.| Isotoop | RA(%) | Halveringstijd | Verval | VE(MeV) | Vervalproducten |
|---|---|---|---|---|---|
| 106Cd | 1,25 | Stabiel met 58 neutronen | --- | --- | --- |
| 107Cd | Synthetisch | 6,5 uur | EV | 1,42 | 107Ag |
| 108Cd | 0,89 | Stabiel met 60 neutronen | --- | --- | --- |
| 109Cd | synthetisch | 463 dagen | EV | 0,21 | 109Ag |
| 110Cd | 12,5 | Stabiel met 62 neutronen | --- | --- | --- |
| 111Cd | 12,8 | Stabiel met 63 neutronen | --- | --- | --- |
| 112Cd | 24,1 | Stabiel met 64 neutronen | --- | --- | --- |
| 113Cd | 12,2 | 7,7x10↑15 jaar | béta | 0,32 | 113In |
| 114Cd | 28,7 | Stabiel met 66 neutronen | --- | --- | --- |
| 115Cd | Synthetisch | 53,5 uur | béta | 1,5 | 115In |
| 116Cd | 7,5 | Stabiel met 68 neutronen | --- | --- | --- |
Voorkomen van Cadmium in de aardkorst
Cadmium is een bijproduct van vooral de zinkwinning. 10% van het cadmium is afkomstig uit recycling van batterijen en andere cadmiumhoudende productenToepassingen van cadmium
- In laagsmeltende legeringen zoals soldeer. Cadmium vormt een legering met zilver, die bekend staat als zilversoldeer en dat voorzichtig behandeld moet worden om cadmium vergiftiging te voorkomen.
- Cadmium als legeringselement in slijtvaste legeringen met grote weerstand tegen metaalmoeheid.
- Cadmium wordt gebruikt als fosforescent in televisiebuizen, cadmiumverbindingen als blauwe en groene kleuren in televisies.
- Cadmiumsulfide CdS is een halfgeleider.
- Cadmiumverbindingen worden als verfkleurstof gebruikt.
- Cadmium wordt gebruikt in het lagermetaal Woodsmetaal.
- Cadmium wordt gebruikt in oplaadbare nikkel-cadmium batterijen.
- Cadmium wordt op andere metalen aangebracht door electroplating (cadmeren), als beschermingslaag tegen corrosie.
- Cadmium absorbeert neutronen en wordt gebruikt als regelstaven in nucleaire reactoren om de snelheid van de reactie te regelen.
Invloed van cadmium op milieu en gezondheid
Lage concentraties cadmium en cadmiumverbindingen kunnen al giftig zijn omdat ze zich ophopen in organismen. Contact met cadmium is niet onmiddellijk schadelijk maar bij veelvuldige blootstelling wel op langere termijn.Cadmium concentraties
- Cadmium komt vrij bij gebruik van fosfaatkunstmeststof en pesticiden, een deel van het cadmium eindigt in de bodem, de rest komt terecht in oppervlaktewater. In slib opgenomen cadmium wordt over grote gebieden verspreid.
- Wormen, bodemorganismen en micro-organismen zijn gevoelig voor cadmiumvergiftiging. Ze sterven bij reeds bij relatief kleine concentraties met als gevolg dat de vruchtbaarheid van de grond terug loopt.
- Putwater uit vervuilde gebieden bevat cadmium, cadmiumrijke stofdeeltjes worden door inslikken of inademen opgenomen in het lichaam.
- Cadmium uitstoot door verbrandingsovens, door verbranden van cadmiumhoudende batterijen en in crematoria.
- Rokers staan bloot aan hoge concentraties cadmium. Tabaksrook komt in de longen en wordt via het bloed naar de rest van het lichaam gepompt. Eén sigaret bevat gemiddeld 1,5 µg cadmium, hiervan wordt circa 10% geïnhaleerd.
- Mensen worden blootgesteld aan cadmium in de buurt van afvalstort, fabrieken die cadmium verwerken en in en nabij metaalraffinaderijen.
Cadmium opname door de mens
De opname van cadmium vindt vooral plaats via het voedsel. Voedsel dat rijk is aan cadmium zijn bijvoorbeeld lever, paddenstoelen, schelpdieren, cacaopoeder en zeewier, ook in bladgroenten als sla en spinazie kan zich cadmium ophopen. Cadmium komt in de lever, bindt zich aan eiwitten die naar de nieren getransporteerd worden, hoopt zich op in de nieren en beschadigt het filtermechanisme. Cadmium hecht aan organisch materiaal in de bodem, waardoor de opname via het voedsel vergroot wordt. In zure bodems nemen planten gemakkelijker cadmium op. Koeien kunnen een relatief grote hoeveelheid cadmium in de nieren hebben. Cadmium hoopt zich op in mossels, oesters, garnalen, kreeften, krabben en vissen. Zout water organismen hebben meer weerstand hebben tegen cadmiumvergiftiging dan zoet water organismen.
Kanker door cadmium en zijn verbindingen
Ingeademd en oraal opgenomen cadmium beschadigt nieren, lever en luchtwegen en verzwakt de beenderen. Veel cadmiumverbindingen zijn kankerverwekkend. De opname van stof moeten we beperken door nat te poetsen, of een stofzuiger gebruiken met speciale filter, de bodem in de omgeving van de woning te beplanten of te bedekken met houtschors om opwaaien te voorkomen; voeten vegen bij het naar binnen gaan.
Gezondheidsklachten door cadmium veroorzaakt
- Diarree, buikpijn en overgeven
- Botbreuk
- Falen van de voortplanting en mogelijk onvruchtbaarheid
- Schade aan het centrale zenuwstelsel
- Schade een het immuunsysteem
- Psychische stoornissen
- DNA schade
 Cadmium /
Cadmium /