Periodiek systeem van elementen
 De essentie van het periodiek systeem is dat het op een overzichtelijke en functionele wijze alle elementen (atomen) omvat die in het universum voorkomen. Het systeem is ontworpen op bases van het groeperen van elementen die onderling vergelijkbaar gedrag vertonen. Zo ontstaat een indeling in blokken, groepen (kolommen) en reeksen. De chemicus schat de eigenschappen van een element in door de plaats die het inneemt in het periodiek systeem en zo konden in het verleden nieuwe elementen voorspeld worden door de plaats van een open plek in het systeem. Het periodiek systeem moet als bases van de chemie beschouwd worden.
De essentie van het periodiek systeem is dat het op een overzichtelijke en functionele wijze alle elementen (atomen) omvat die in het universum voorkomen. Het systeem is ontworpen op bases van het groeperen van elementen die onderling vergelijkbaar gedrag vertonen. Zo ontstaat een indeling in blokken, groepen (kolommen) en reeksen. De chemicus schat de eigenschappen van een element in door de plaats die het inneemt in het periodiek systeem en zo konden in het verleden nieuwe elementen voorspeld worden door de plaats van een open plek in het systeem. Het periodiek systeem moet als bases van de chemie beschouwd worden. Het periodiek systeem van elementen. De indeling is gebaseerd op de eigenschappen van de elementen. / Bron: Cepheus, Wikimedia Commons (Publiek domein)
Het periodiek systeem van elementen. De indeling is gebaseerd op de eigenschappen van de elementen. / Bron: Cepheus, Wikimedia Commons (Publiek domein)De blokken van het periodiek systeem
Een blok van het periodiek systeem verwijst naar de buitenbaan (orbitaal) die wordt opgevuld met valentie-elektronen, dat zijn de elektronen die actief deelnemen aan chemische reacties.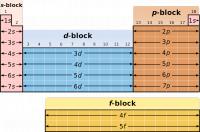 Periodiek systeem Ingedeeld in blokken / Bron: Roshan220195, Wikimedia Commons (CC BY-SA-3.0)
Periodiek systeem Ingedeeld in blokken / Bron: Roshan220195, Wikimedia Commons (CC BY-SA-3.0)- s-blok
- p-blok
- d-blok
- f-blok
De namen van de blokken (s, p, d, f, ) zijn afgeleid van de kwaliteit van de spectroscopische lijnen van de atoomschillen: (s)sharp, (p) principal, (d) diffuse en (f) fundamenteel.
s-blok
Het s-blok omvat de chemische elementen waarin een s-subschil wordt opgevuld, dit zijn de kolommen 1 en 2 van het periodiek systeem, namelijk de
p-blok
Chemische elementen die in hun grondtoestand een gedeeltelijk gevulde p-subschil (gevuld met 1 tot 5 elektronen) hebben. Dit zijn de kolommen 13 tot en met 17 van het periodiek systeem: de boorgroep (B), de koolstofgroep(C), de stikstofgroep(N), de zuurstofgroep(O) en de fluor(halogenen)groep(F).
d- blok
Overgangsmetalen zijn de elementen uit het d-blok. Men onderscheidt:
- de 3d-overgangsmetalen van scandium tot zink
- de 4d-overgangsmetalen van yttrium tot cadmium
- de 5d-overgangsmetalen van hafnium tot kwik
- de 6d-overgangsmetalen van rutherfordium tot copernicium
f-blok
Het f-blok wordt gevormd door die elementen in het periodiek systeem waarin de f-subschil geheel of gedeeltelijk wordt opgevuld. Het zijn de lanthaniden (4f subschil) en actiniden (5f subschil).
Periodiek systeem van elementen
Door op de chemische symbolen te klikken van onderstaand periodiek systeem, verschijnt het hoofdartikel van het element in beeld. De Lanthaniden(*) en de Actiniden(**) moeten in gedachten geschoven worden in de open plaatsen *en ** in het systeem. Door op de (R) onder het element symbool te klikken wordt de elementenreeks (een special) opgeroepen waartoe het element behoort.| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | Peri- ode↓ |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 1 H R | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD]2 He R | 1 | |||||||||
| 3 Li R | 4 Be R | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | 5 B R | 6 C R | 7 N R | 8 O R | 9 F R | 10 Ne R | 2 | |||||
| 11 Na R | 12 Mg R | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | [/TD][TD] | 13 Al R | 14 Si R | 15 P R | 16 S R | 17 Cl R | 18 Ar R | 3 | |||||
| 19 K R | 20 Ca R | 21 Sc R | 22 Ti R | 23 V R | 24 Cr R | 25 Mn R | 26 Fe R | 27 Co R | 28 Ni R | 29 Cu R | 30 Zn R | 31 Ga R | 32 Ge R | 33 As R | 34 Se R | 35 Br R | 36 Kr R | 4 |
| 37 Rb R | 38 Sr R | 39 Y R | 40 Zr R | 41 Nb R | 42 Mo R | 43 Tc R | 44 Ru R | 45 Rh R | 46 Pd R | 47 Ag R | 48 Cd R | 49 In R | 50 Sn R | 51 Sb R | 52 Te R | 53 J R | 54 Xe R | 5 |
| 55 Cs R | 56 Ba R | * | 72 Hf R | 73 Ta R | 74 W R | 75 Re R | 76 Os R | 77 Ir R | 78 Pt R | 79 Au R | 80 Hg R | 81 Tl R | 82 Pb R | 83 Bi R | 84 Po R | 85 At R | 86 Rn R | 6 |
| 87 Fr R | 88 Ra R | ** | 104 Rf R | 105 Db R | 106 Sg R | 107 Bh R | 108 Hs R | 109 Mt R | 110 Ds R | 111 Rg R | 112 Cn R | 113 Uut R | 114 Fl R | 115 Uup R | 116 Lv R | --- | --- | 7 |
| [/TD][TD]* | 57 La R | 58 Ce R | 59 Pr R | 60 Nd R | 61 Pm R | 62 Sm R | 63 Eu R | 64 Gd R | 65 Tb R | 66 Dy R | 67 Ho R | 68 Er R | 69 Tm R | 70 Yb R | 71 Lu R | |||
| [/TD][TD]** | 89 Ac R | 90 Th R | 91 Pa R | 92 U R | 93 Np R | 94 Pu R | 95 Am R | 96 Cm R | 97 Bk R | 98 Cf R | 99 Es R | 100 Fm R | 101 Md R | 102 No R | 103 Lr R |
Chemische reeksen (R) in het periodiek systeem op volgorde van atoomnummer
Door in onderstaande overzicht de naam van een reeks aan te slaan komt de special te voorschijn die deze reeks van elementen behandelt.| Alkalimetalen | Aardalkalimetalen | overgangsmetalen | Hoofdgroepmetalen | Metalloiden |
| Niet-metalen | Halogenen | Edelgassen | Lanthaniden | Actiniden |
Lijst van chemische elementen in volgorde van atoomnummer
Het zoeken van elementen in het periodiek systeem is voor niet chemici een doolhof en voor de namen van de elementen is bovendien te weinig ruimte in het systeem. Deze lijst van elementen is geordend volgens het atoomnummer. De klik optie voor een alfabetische volgorde wordt er nog aan toegevoegd.| Nr | Naam | Symbool | Nr | Naam | Symbool | Nr | Naam | Symbool |
|---|---|---|---|---|---|---|---|---|
| 1 | Waterstof | H | 41 | Niobium | Nb | 81 | Thalium | Tl |
| 2 | Helium | He | 42 | Molybdeen | Mo | 82 | Lood | Pb |
| 3 | Lithium | Li | 43 | Technetium | Tc | 83 | Bismuth | Bi |
| 4 | Beryllium | Be | 44 | Ruthenium | Ru | 84 | Polonium | Po |
| 5 | Bohrium | B | 45 | Rhodium | Rh | 85 | Astatium | At |
| 6 | Koolstof | C | 46 | Palladium | Pd | 86 | Radon | Rn |
| 7 | Stikstof | N | 47 | Zilver | Ag | 87 | Francium | Fr |
| 8 | Zuurstof | O | 48 | Cadmium | Cd | 88 | Radium | Ra |
| 9 | Fluor | F | 49 | Indium | In | 89 | Actinium | Ac |
| 10 | Neon | Ne | 50 | Tin | Sn | 90 | Thorium | Th |
| 11 | Natrium | Na | 51 | Antimoon | Sb | 91 | Protactinium | Pa |
| 12 | Magnesium | Mg | 52 | Tellurium | Te | 92 | Uranium | U |
| 13 | Aluminium | Al | 53 | Jodium | J | 93 | Neptunium | Np |
| 14 | Silicium | Si | 54 | Xenon | Xe | 94 | Plutonium | Pu |
| 15 | Fosfor | P | 55 | Cesium | Cs | 95 | Americum | Am |
| 16 | Zwavel | S | 56 | Barium | Ba | 96 | Curium | Cm |
| 17 | Chloor | Cl | 57 | Lanthanium | La | 97 | Berkelium | Bk |
| 18 | Argon | Ar | 58 | Cerium | Ce | 98 | Californium | Cf |
| 19 | Kalium | K | 59 | Praseodynium? | Pr | 99 | Einsteinium | Es |
| 20 | Calcium | Ca | 60 | Neodynium? | Nd | 100 | Fermium | Fm |
| 21 | Scandium | Sc | 61 | Promethium | Pm | 101 | Mendelevium | Md |
| 22 | Titanium | Ti | 62 | Samarium | Sm | 103 | Lawrencium | Lr |
| 23 | Vanadium | V | 63 | Europium | Eu | 104 | Rutherfordium | Rf |
| 24 | Chroom | Cr | 64 | Gadolinium | Gd | 105 | Dubnium | Db |
| 25 | Mangaan | Mn | 65 | Terbium | Tb | 106 | Seaborgium | Sg |
| 26 | IJzer | Fe | 66 | Dysprosium | Dy | 107 | Bohrium | Bh |
| 27 | Kobalt | Co | 67 | Holmium | Ho | 108 | Hassium | Hs |
| 28 | Nikkel | Ni | 68 | Erbium | Er | 109 | Meitnerum | Mt |
| 29 | Koper | Cu | 69 | Thulium | Tm | 110 | Darmstadtum | Ds |
| 30 | Zink | Zn | 70 | Ytterbium | Yb | 111 | Roentgenium | Rg |
| 31 | Gallium | Ga | 71 | Lutetium | Lu | 112 | Copernicum | Cn |
| 32 | Germanium | Ge | 72 | Hafnium | Hf | 113 | Ununtrium | Uut |
| 33 | Arsenicum | As | 73 | Tantalium | Ta | 114 | Flevium | Fl |
| 34 | Seleen | Se | 74 | Wolfraam | W | 115 | Ununpentium | Uup |
| 35 | Broom | Br | 75 | Renium | Re | 116 | Livermorium | Lv |
| 36 | Krypton | Kr | 76 | Osmium | Os | 117 | Ununseptium | Uus |
| 37 | Rubidiun | Rb | 77 | Iridium | Ir | 118 | Ununoctium | Uuo |
| 38 | Strontium | Sr | 78 | Platina | Pt | |||
| 39 | Yttrium | Y | 79 | Goud | Au | |||
| 40 | Zirkonium | Zr | 80 | Kwik | Hg |