Elektronenconfiguratie: De mantel van het atoom
 Bohr verklaarde met zijn atoommodel in 1913 dat elektronen in de buitenste elektronenschil de chemische eigenschappen van een element bepalen. Bohr stelde zich de elektronenschillen voor als cirkelvormige schalen rond de atoomkern. Elke schil heeft een bepaald energieniveau ten opzichte van de kern, de binnenste schillen hebben een lager energieniveau dan de buitenste, dat houdt in dat elektronen in beginsel eerst de banen dicht bij de kern bezetten. De elektronen beïnvloeden elkaar echter vandaar dat er uitzonderingen bestaan op de regel dat de binnenste schillen het eerst helemaal gevuld worden. De beschrijving van de elektronenconfiguratie met de qauntummechanica valt buiten het bestek van dit artikel.
Bohr verklaarde met zijn atoommodel in 1913 dat elektronen in de buitenste elektronenschil de chemische eigenschappen van een element bepalen. Bohr stelde zich de elektronenschillen voor als cirkelvormige schalen rond de atoomkern. Elke schil heeft een bepaald energieniveau ten opzichte van de kern, de binnenste schillen hebben een lager energieniveau dan de buitenste, dat houdt in dat elektronen in beginsel eerst de banen dicht bij de kern bezetten. De elektronen beïnvloeden elkaar echter vandaar dat er uitzonderingen bestaan op de regel dat de binnenste schillen het eerst helemaal gevuld worden. De beschrijving van de elektronenconfiguratie met de qauntummechanica valt buiten het bestek van dit artikel.Het neutrale atoom
Het massagetal (A) is het totale aantal protonen en neutronen (som der nucleonen) in een atoomkern. Atoomnummer (Z) is het aantal protonen in de kern. Het verschil tussen het massagetal en atoomnummer geeft het aantal neutronen (N) in een bepaalde nucleus. N = A - ZVoor een neutraal atoom geldt:
Atoomnummer Z = Aantal protonen = Aantal elektronen
Aantal neutronen N = Massagetal A (totaal aantal nucleonen) - Atoomnummer Z (aantal protonen)
Elektronenconfiguratie
De elektronenconfiguratie van een atoom geeft de verdeling weer van de elektronen over de verschillende hoofdschillen en subschillen (banen) rond de atoomkern. De elektronenconfiguratie tabel laat zien hoeveel elektronen(banen) er in elk energieniveau n zitten en de verdeling van de elektronen over de subschillen.Elektronenconfiguratie tabel
Als voorbeeld neemt men het goudatoom. s, p, d, f zijn de subschillen (baantypen) binnen de energieniveaus n = 2, 3, 4, 5, 6. Het totale aantal elektronen per energieniveau is de som van de elektronen in de subschillen van dat energieniveau n. Het aantal elektronen per energieniveau 1 t/m 6 in een goudatoom is in onderstaande tabel weergegeven. Het maximum aantal elektronen dat een energieniveau kan bezetten wordt gevonden met de formule 2n², waarin n het hoofdquantum getal. De verschillende stabiele elektronenbanen worden bepaald door het golfkarakter van de elektronbeweging, waarbij de golflengte λ wordt bepaald door λ=h/mv, waarin h de constante van Planc, m de massa van het elektron en v zijn baansnelheid. Omdat de baanomtrek gedeeld door de golflengte een geheel getal is, kunnen zich alleen bepaalde banen instellen.
| n | s | p | d | f | Goud: Aantal elektronen op energieniveau n | Goud: Maximaal aantal elektronen op energieniveau n = 2n2 |
|---|---|---|---|---|---|---|
| 1 | 1s2 | --- | --- | --- | 2 | 2 |
| 2 | 2s2 | 2p6 | --- | --- | 8 | 8 |
| 3 | 3s2 | 3p6 | 3d10 | -- | 18 | 18 |
| 4 | 4s2 | 4p6 | 4d10 | 4f14 | 32 | 32 |
| 5 | 5s2 | 5p6 | 5d10 | --- | 18 | 50 |
| 6 | 6s1 | --- | --- | --- | 1 | 72 |
 Bron: Roshan220195, Wikimedia Commons (CC BY-SA-3.0)
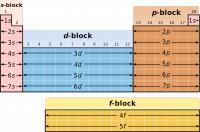
Bron: Roshan220195, Wikimedia Commons (CC BY-SA-3.0)Blokken in periodiek systeem
Het type blok verwijst naar het baantype dat wordt gevuld met valentie-elektronen. De blokken zijn:- s-blok
- p-blok
- d-blok
- f-blok
De chemische eigenschappen, d.w.z. het gedrag van atomen uit hetzelfde blok vertonen duidelijke overeenkomsten. De chemische eigenschappen van de atomen worden namelijk grotendeels bepaald door de buitenelektronen (valentie-elektronen).
Elektronegativiteit volgens de Paulingschaal
Elektronegativiteit is een maat voor de bereidheid van een atoom om elektronen van buiten aan te trekken. Elementen aan de rechterkant van het periodiek systeem zijn elektronegatief (2,5-4) en die aan de linkerkant zijn elektropositief (0,8-1,5)t.o.v. de atomen van de rechterkant.Elektronenaffiniteit
De elektronenaffiniteit van atoom of molecuul is de vrijkomende energie bij de opname van een elektron door een neutraal atoom. Positieve elektronenaffiniteit betekent dat er energie vrijkomt bij de overgang van atoom naar anion. (anion is een negatief geladen ion, het atoom vangt dus een elektron in en de kinetische energie van dat elektron is de energie toename). Chloor trekt het sterkst een extra elektron aan en kwik trekt het zwakst een extra elektron aan. De elektronenaffiniteit van edelgassen is ongeveer 0. Niet-metalen hebben door de bank genomen een grotere elektronenaffiniteit dan metalen.Ionisatiepotentiaal
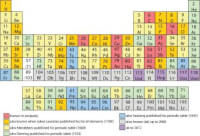
De ionisatiepotentiaal of -energie is een maat voor de bindingsenergie van een elektron aan het atoom en dat is de energie die nodig is om uit een vrij atoom een elektron te stoten. Ionisatiepotentiaal in volts, of ionisatie-energie in Joule of elektronvolt, of molaire ionisatie-energie (Joule per mol).De ionisatiepotentialen van de elementen tonen de periodieke structuur van de atoomopbouw met zijn regelmatig terugkerende elektronenconfiguraties, volgens grafiek eV=Functie(Z). Edelgassen met hun volledig gevulde schillen hebben de hoogste potentialen en alkalimetalen de laagste.
 Bron: Sandbh, Wikimedia Commons (CC BY-SA-3.0)
Bron: Sandbh, Wikimedia Commons (CC BY-SA-3.0) Bron: PNG: w:de:user:Kiko2000; SVG: Cepheiden, Wikimedia Commons (CC BY-SA-3.0)
Bron: PNG: w:de:user:Kiko2000; SVG: Cepheiden, Wikimedia Commons (CC BY-SA-3.0)