Bereiding en standaardisatie van een dijood-oplossing
 Een dijood-oplossing kan worden gebruikt als indicator om zetmeel aan te tonen. In aanwezigheid van zetmeel krijgt dijood immers een intens blauwe kleur. Deze indicator-eigenschap kan ook worden aangewend bij jodo-jodimetrische concentratiebepalingen. Voor rechtstreekse jodo-jodimetrie-titraties zijn dijood-oplossingen met een exact gekende concentratie nodig. Dijood-oplossingen vragen echter een specifieke bereiding en standaardisatie.
Een dijood-oplossing kan worden gebruikt als indicator om zetmeel aan te tonen. In aanwezigheid van zetmeel krijgt dijood immers een intens blauwe kleur. Deze indicator-eigenschap kan ook worden aangewend bij jodo-jodimetrische concentratiebepalingen. Voor rechtstreekse jodo-jodimetrie-titraties zijn dijood-oplossingen met een exact gekende concentratie nodig. Dijood-oplossingen vragen echter een specifieke bereiding en standaardisatie.
- Jodo-jodimetrie
- Bereiding van een I2 oplossing
- Standaardisatie van de I2-oplossing
- Uitgewerkt voorbeeld
Jodo-jodimetrie
I2 + reductor → 2I- + geoxideerde vorm van de reductor
Bereiding van een I2 oplossing
I2 is een apolaire stof en is dus niet oplosbaar in water. Toch is het mogelijk om een waterige I2-oplossing te maken. Door KI (gedissocieerd: K+ + I-) toe voegen wordt het polaire I3- gevormd. Het vertoont dezelfde eigenschappen als I2 maar is dus wel oplosbaar in water.I2 + I- → I3-
Voor de bereiding van een I2-oplossing met gekende concentratie wordt dus de juiste massa I2 afgewogen en wordt er een massa KI toegevoegd die minstens twee keer zo groot is. Het gehalte I- (het teveel aan KI dus) dat niet betrokken is in de vorming van I3- zal geen invloed hebben op de concentratie van de oplossing.
Standaardisatie van de I2-oplossing
I2 is geen oertiterstof en I2-oplossingen dienen dus te worden gestandaardiseerd. I2 heeft als eigenschap dat het makkelijk sublimeert, wat betekent dat het vanuit de vaste toestand als gas vervliegt. Tijdens het afwegen van I2 zal er dus steeds wat I2 verloren gaan in de lucht. Standaardisatie is dus nodig om de exacte concentratie van de bereide oplossing te kennen. Een I2-oplossing kan worden gestandaardiseerd met een natriumthiosulfaat (Na2S2O3)-oplossing met gekende concentratie.I2 + 2S2O32- → 2I- + S4O62-
Natriumthiosulfaat is echter ook geen oertiterstof en ook deze oplossingen dienen dus te worden gestandaardiseerd. De standaardisatie van een thiosulfaat-oplossing kan worden uitgevoerd met de oertiterstof kaliumjodaat (KIO3). Bij deze standaardisatie dient ook een overmaat aan KI te worden toegevoegd. De reactie verloopt in 2 stappen.
- 12H+ + 2IO3- + 10I- → 6I2 + 6H2O
- 6I2 + 12S2O32- → 12I- + 6S4O62-
Globale reactie:
1 + 2: 6H+ + IO3- + 6S2O32- → 3H2O + I- + 3S4O62-
1 + 2: 6H+ + IO3- + 6S2O32- → 3H2O + I- + 3S4O62-
Uitgewerkt voorbeeld
Standaardisatie van een I2-oplossing (0.004 mol/L) met een Na2S2O3-oplossing (0.008 mol/L)Bereiding en standaardisatie van de Na2S2O3-oplossing
- Weeg de juiste hoeveelheid Na2S2O3 af om 0.250 L oplossing te bereiden.
- nNa2S2O3 = cNa2S2O3 x V = 0.008 mol/L x 0.250 L = 0.002 mol
- mNa2S2O3 = nNa2S2O3 x MNa2S2O3 = 0.002 mol x 158.097 g/mol = 0.316 g
- Breng deze massa Na2S2O3 in een maatkolf van 0.250L en leng aan met demiwater.
- Weeg 10 mg KIO3 af en breng dit over in een erlenmeyer van bijvoorbeeld 300 mL.
- nKIO3 = mKIO3 / MKIO3 = 0.010 g / 213.997 g = 4.7 x 10-5 mol
- Verdun met demiwater tot ongeveer 50 mL.
- Laat de KIO3 oplossen, eventueel onder verwarmen.
- Voeg 0,16 g KI toe en laat dit ook oplossen.
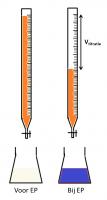
- Voeg tenslotte 10 mL van een geconcentreerde HCl-oplossing toe en titreer onmiddellijk het vrijgekomen I2 met de thiosulfaatoplossing, tot de oplossing lichtgeel kleurt.
- Voeg dan 5 mL zetmeeloplossing toe en titreer verder tot de oplossing kleurloos is.
Stel Vtitratie = 0.035 L
- nNa2S2O3 = nKIO3 x 6 = 4.7 x 10-5 x 6 = 2.8 x 10-4 mol
- cNa2S2O3 = 2.8 x 10-4 mol / 0.035 L = 0.008 mol/L
Bereiding en standaardisatie van de I2-oplossing
- Weeg de juiste hoeveelheid I2 af om 0.250 L oplossing te bereiden.
- nI2 = cI2 x V = 0.004 mol/L x 0.250 L = 0.001 mol
- mI2 = nI2 x MI2 = 0.001 mol x 253.8 g/mol = 0.254 g
- Voeg een massa twee keer zo groot aan KI toe.
- Leng aan met demiwater en roer om zoveel mogelijk I2 in oplossing te krijgen.
- Filtreer.
- Stel 0.025 L van de oplossing (filtraat) met de gestandaardiseerde Na2S2O3-oplossing.
Stel Vtitratie = 0.020 L
- nNa2S2O3 = 0.008 mol/L x 0.020 L = 0.00016 mol
- nI2 = nNa2S2O3 / 2 = 0.00016 mol / 2 = 0.00008 mol
- cI2 = 0.00008 mol / 0.020 L = 0.004 mol/L
© 2020 - 2024 Guust2016, het auteursrecht van dit artikel ligt bij de infoteur. Zonder toestemming is vermenigvuldiging verboden. Per 2021 gaat InfoNu verder als archief, artikelen worden nog maar beperkt geactualiseerd.
 Stappenplan: de vergelijking voor een redoxreactie opstellenEen redoxreactie is een reactie waarbij elektronen worden uitgewisseld. Het kan gaan om een reactie tussen atomen, molec…
Stappenplan: de vergelijking voor een redoxreactie opstellenEen redoxreactie is een reactie waarbij elektronen worden uitgewisseld. Het kan gaan om een reactie tussen atomen, molec…
 Bleekwater en zure ontkalker, een gevaarlijke chloorcocktailBleekwater (of javel) bevat hypochlorietionen (ClO-) die als sterke oxidator fungeren t.o.v. kleurstoffen (bleekwater) e…
Bleekwater en zure ontkalker, een gevaarlijke chloorcocktailBleekwater (of javel) bevat hypochlorietionen (ClO-) die als sterke oxidator fungeren t.o.v. kleurstoffen (bleekwater) e…
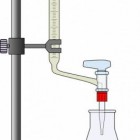 De werking van een redoxindicatorOm het equivalentiepunt bij een redoxtitratie met kleurloze of weinig gekleurde oplossingen te kunnen zien, dient een re…
De werking van een redoxindicatorOm het equivalentiepunt bij een redoxtitratie met kleurloze of weinig gekleurde oplossingen te kunnen zien, dient een re…
 De werking van een lampje in een reddingsvestReddingsvesten zijn vaak uitgerust met een lampje. Bij bepaalde uitvoeringen is dat lampje via stroomdraadjes verbonden…
De werking van een lampje in een reddingsvestReddingsvesten zijn vaak uitgerust met een lampje. Bij bepaalde uitvoeringen is dat lampje via stroomdraadjes verbonden…
 Permanganometrie: redoxtitraties met kaliumpermanganaatPermanganometrie is een verzamelnaam voor redoxtitraties waarbij als titrant kaliumpermanganaat wordt gebruikt. In water…
Permanganometrie: redoxtitraties met kaliumpermanganaatPermanganometrie is een verzamelnaam voor redoxtitraties waarbij als titrant kaliumpermanganaat wordt gebruikt. In water…
 De belangrijkste concentratie-eenheden op een rijtjeIn wetenschappelijk onderzoek wordt er voor oplossingen meestal de concentratie-eenheid mol/L gebruikt. In het dagelijks…
De belangrijkste concentratie-eenheden op een rijtjeIn wetenschappelijk onderzoek wordt er voor oplossingen meestal de concentratie-eenheid mol/L gebruikt. In het dagelijks…
Gerelateerde artikelen
Bronnen en referenties
- Inleidingsfoto: OpenClipart-Vectors, Pixabay
- Binas, Wolters, Noordhoff
Guust2016 (74 artikelen)
Gepubliceerd: 19-11-2020
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Gepubliceerd: 19-11-2020
Rubriek: Wetenschap
Subrubriek: Scheikunde
Bronnen en referenties: 2
Per 2021 gaat InfoNu verder als archief. Het grote aanbod van artikelen blijft beschikbaar maar er worden geen nieuwe artikelen meer gepubliceerd en nog maar beperkt geactualiseerd, daardoor kunnen artikelen op bepaalde punten verouderd zijn. Reacties plaatsen bij artikelen is niet meer mogelijk.